
| A. | 铅蓄电池反应为Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O,放电时负极质量减轻 | |
| B. | 电解精炼铜时,以粗铜作阴极,纯铜作阳极 | |
| C. | CH3COONa稀溶液加水稀释后,溶液中$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$ 的值增大 | |
| D. | CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 |
分析 A.原电池放电时,正极发生还原反应,电极反应是PbO2+4H++SO42--2e-=2H2O+PbSO4,负极为Pb+SO42--2e-=PbSO4;
B.电解法精炼粗铜,粗铜做阳极,精铜做阴极,含铜离子的盐溶液做电解质溶液;
C.CH3COONa溶液中存在CH3COO-+H2O?CH3COOH+OH-,加水促进水解;
D.反应自发进行的判断依据是△H-T△S<0.
解答 解:A.根据负极Pb+SO42--2e-=PbSO4知,放电过程中负极质量增加,增加的质量为硫酸根离子的质量,故A错误;
B.电解法精炼粗铜,用纯铜作阴极,用粗铜作阳极,用纯铜作阴极,在该电极上会析出大量的铜,故B错误;
C.CH3COONa溶液中存在CH3COO-+H2O?CH3COOH+OH-,加水促进水解,CH3COOH的物质的量在增加,CH3COO-的物质的量在减小,体积相同,溶液中$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$ 的值增大,故C正确;
D.CaCO3(s)═CaO(s)+CO2(g)室温下不能自发进行,反应△S>0,△H-T△S>0,说明该反应的△H>0,故D错误;
故选C.
点评 本题考查铅蓄电池反应、精炼粗铜、盐类水解、自发反应等知识,题目难度不大,掌握电化学知识以及注意反应自发进行的判断依据是△H-T△S<0为解答关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
 常温下,向100mL 0.01mol•L-1 MOH溶液中逐滴加入0.02mo1•L-1 HA溶液,图中所示曲线表示混合溶液的pOH变化情况(溶液体积变化忽略不计),溶液中pOH=-lgc(OH-).下列说法中,不正确的是( )
常温下,向100mL 0.01mol•L-1 MOH溶液中逐滴加入0.02mo1•L-1 HA溶液,图中所示曲线表示混合溶液的pOH变化情况(溶液体积变化忽略不计),溶液中pOH=-lgc(OH-).下列说法中,不正确的是( )| A. | MOH为一元强碱 | |
| B. | N点水的电离程度大于K点水的电离程度 | |
| C. | 该温度下HA的电离平衡常数为5×10-6mo1•L-1 | |
| D. | 若K点对应溶液的pOH=10,则有c(HA)+c(H+)-c(OH-)=0.01mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广使用清洁能源 | B. | 大力发展燃煤发电 | ||
| C. | 循环高效利用费源 | D. | 倡导环保低碳生活 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W | 某种氧化物是淡黄色固体 |
| X | 短周期中最高价氧化物对应水化物酸性最强 |
| Y | 第三周期中离子半径最小的 |
| Z | 原子最外层电子数是电子总数的$\frac{2}{3}$ |
| A. | W、Y、X的原子半径依次减小,Y、W、X简单离子的半径依次增大 | |
| B. | W、X、Y的最高价氧化物的水化物之间可以两两反应 | |
| C. | W的氧化物与Z的最高价氧化物反应一定是氧化还原反应 | |
| D. | 金属性W比Y强,非金属性Z比X弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 工业上用CO和H2生产燃料甲醇.一定条件下密闭容器中发生反应,测得数据曲线如图所示(反应混合物均呈气态).下列说法错误的是( )
工业上用CO和H2生产燃料甲醇.一定条件下密闭容器中发生反应,测得数据曲线如图所示(反应混合物均呈气态).下列说法错误的是( )| A. | 反应的化学方程式:CO+2H2?CH3OH | |
| B. | 反应进行至3分钟时,正、逆反应速率相等 | |
| C. | 反应至10分钟,?(CO)=0.075 mol/L•min | |
| D. | 增大压强,平衡正向移动,K不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①中加人试剂顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液 | |
| B. | 过程②为电解熔融精盐 | |
| C. | 工业上过程③加入的试剂为浓NaOH溶液 | |
| D. | 第④步反应的离子方程式可表示为:2Br-+Cl2=Br2+2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
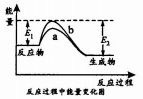
| A. | △H=+|E1-E2| | |
| B. | 曲线a为催化剂时的反应 | |
| C. | X(g)的能量高于Z(g)的能量 | |
| D. | 反应物吸收的总能量大于生成物释放的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na+O2$\frac{\underline{\;点燃\;}}{\;}$Na2O2 | B. | Na2O+H2O═2NaOH | ||
| C. | 2F2+2H2O═4HF+O2 | D. | 2C+SiO2$\frac{\underline{\;高温\;}}{\;}$2CO↑+Si |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该废水中可能含有较多的Fe2+、Fe3+ | |
| B. | 此电解法缺点之一是会产生少量氯气 | |
| C. | 阳极反应式为2CN--10e-+3H2O=CO2↑+N2↑+6H+ | |
| D. | 电解法处理后的废水pH减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com