
| A. | NaAlO2溶液 | B. | Na2SiO3溶液 | C. | 漂白粉溶液 | D. | CaCl2 |
分析 A.二氧化碳通入NaAlO2溶液中反应生成氢氧化铝白色沉淀;
B.二氧化碳与水玻璃反应生成硅酸;
C.二氧化碳通入漂白粉溶液中发生反应生成碳酸钙沉淀和次氯酸;
D.二氧化碳与氯化钙不反应.
解答 解:A.二氧化碳通入NaAlO2溶液中反应生成氢氧化铝白色沉淀,故A不选;
B.二氧化碳与水玻璃反应生成硅酸,硅酸不溶于水,是白色胶状沉淀,反应过程现象明显,故B不选;
C.二氧化碳通入漂白粉溶液中发生反应生成碳酸钙沉淀和次氯酸,故C不选;
D.二氧化碳与氯化钙不反应,没有明显现象,整个过程中无明显现象,故D选;
故选D.
点评 本题考查钠、氯元素化合物的性质,题目难度不大,清楚发生的反应及物质的性质是关键,注意基础知识的理解掌握.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
| 实验步骤 | 有关问题 |
| (1)计算所需Na2CO3的质量 | 需要Na2CO3的质量为10.6g. |
| (2)称量Na2CO3固体 | 称量过程中主要用到的仪器是托盘天平、砝码、药匙. |
| (3)将Na2CO3加入100mL烧杯中 | 为加快溶解速率,可采取的措施是用玻棒搅拌或加热 |
| (4)将烧杯中的溶液转移至500mL容量瓶中 | 为防止溶液溅出,应采取的措施是用玻璃棒引流 |
| (5)向容量瓶中加蒸馏水至刻度线 | 在进行此操作时应注意的问题是当加水璃刻度线1-2cm时改用胶头璃管加水至凹液面与刻度线相切 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 具有相同电子层数而又按原子序数递增顺序排列的横行称为周期 | |
| B. | 元素周期表共有14列元素:7个主族和7个副族 | |
| C. | 元素周期表的第一列元素称为第IA族,均为活泼的金属元素 | |
| D. | 元素周期表中第二周期第VIIA族元素的最高正价为+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非极性键只存在于双原子的单质分子(如Cl2)中 | |
| B. | 在共价化合物里,可能存在离子键 | |
| C. | 在离子化合物里,只存在离子键,没有共价键 | |
| D. | 化学反应的实质是旧键的断裂,新键的形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 48 mol•(L•s )-1 | B. | 36 mol•(L•s )-1 | C. | 24 mol•(L•s )-1 | D. | 12 mol•(L•s )-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其氢氧化物中碱性最强的是NaOH | B. | 单质还原能力最强的是铯 | ||
| C. | 单质熔点最低的是钠 | D. | 原子半径逐渐减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
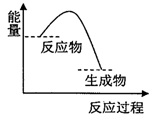
| A. | 该反应过程中,形成新化学键释放的总能量小于断裂旧化学键吸收的总能量 | |
| B. | 因为生成物的总能量低于反应物的总能量,所以该反应不需要加热即可进行 | |
| C. | 该图象可以表示碳酸钙受热分解的能量变化 | |
| D. | 该图象可以表示锌与稀硫酸反应的能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
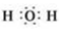 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com