
【题目】分离苯和水需要选用的仪器是
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
【答案】C
【解析】
根据苯和水互不相溶,选择分离的方法。
A. 仪器名称为量筒,可量取一定体积的液体,不能分离苯和水,A项错误;
B. 仪器名称为漏斗,可用于过滤难溶物,不能分离苯和水,B项错误;
C. 仪器名称为分液漏斗,可用于分离互不相溶的混合液体或萃取实验,因苯和水互不相溶,需用分液的方法分离,C项正确;
D. 仪器名称为容量瓶,可用于配制一定浓度的标准溶液,不能分离提纯混合物,D项错误;
答案选C。
方法 | 课本举例 | 分离的物质 |
过滤 | 除去粗盐中的泥沙 | 用水溶解,从溶液中分离出不溶固体物质 |
蒸发 | 从食盐溶液中分离出NaCl | 加热溶液,从溶液中分离出易溶固体溶质 |
蒸馏 | 从自来水制蒸馏水 | 加热并冷凝,从互溶的液态混合物中分离出沸点不同物质 |
萃取 | 用CCl4提取碘水中碘 | 用一种溶剂把溶质从它与另一溶剂组成的溶液中提取出来 |
洗气 | 用饱和食盐水除去氯气中的氯化氢杂质。 | 气体与气体的分离(杂质气体与液体反应)。 |
升华 | 碘的升华 | 分离易升华的物质。 |


科目:高中化学 来源: 题型:
【题目】Atropic 酸(H)是某些具有消炎、镇痛作用药物的中间体,其一种合成路线如下:
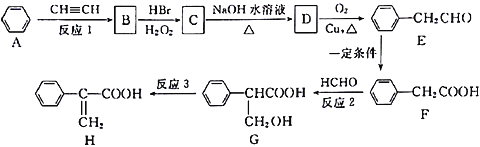
(1)G中含氧官能团的名称是____________;反应1为加成反应,则B的结构简式是________________。
(2)反应2的反应类型为________________,反应3的反应条件为________________。
(3)C→D的化学方程式是________________________________。
(4)写出E与银氨溶液水浴反应的离子方程式_______________________________。
(5)下列说法正确的是________。
a. B中所有原子可能在同一平面上
b. 合成路线中所涉及的有机物均为芳香族化合物
c.一定条件下1mol有机物H最多能与5molH2发生反应
d. G能发生取代、加成、消去、氧化、缩聚等反应
(6)化合物G有多种同分异构体,其中同时满足下列条件:①能发生水解反应和银镜反应; ②能与FeC13发生显色反应;③核磁共振氢谱只有4个吸收峰的同分异构体的结构简式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同物质的量的乙烯和甲烷的下列说法中,不正确的是( )
A.碳原子个数比为 2∶1
B.氢原子个数比为1∶1
C.完全燃烧时,消耗氧气的体积比为2∶3
D.完全燃烧时,生成水的质量比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下,HCOOH(甲酸)比NH3H2O电离常数大。向10 mL 0.1mol/L HCOOH中滴加同浓度的氨水,有关叙述正确的是( )
A. 滴加过程中水的电离程度始终增大
B. 当加入10 mL NH3H2O时,c(NH4+) > c(HCOO-)
C. 当两者恰好中和时,溶液pH = 7
D. 滴加过程中n(HCOOH)与n(HCOO-)之和保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知在常温常压下:
①CH3OH(l)+O2(g)===CO(g)+2H2O(g) ΔH=-354.8 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH=-566.0 kJ·mol-1
③H2O(g)===H2O(l) ΔH=-44.0 kJ·mol-1
则表示CH3OH(l)燃烧热的热化学方程式为______________________________________。
(2)由甲醇、氧气和NaOH溶液构成的新型手机电池,充电一次可使手机连续使用一个月。
①该电池负极的电极反应式为________________________________________________。
②若以该电池为电源,用石墨作电极电解200 mL含有如下离子的溶液。
离子 | Cu2+ | H+ | Cl- | SO42- |
c/(mol·L-1) | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)。阳极上最先发生的反应为___________________________;从各阶段的电解总反应方程式来看,最初是电解__________(填写化学式,下同)溶液,然后是电解________溶液,最后是电解H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠是一种工业盐,在生产、生活中应用广泛。现用下图所示装置(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物成分。
已知:①NO+NO2+2OH-=2NO2-+H2O②气体液化的温度:NO2 21℃、 NO –152℃

(1)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是__________。
(2)该实验装置明显缺陷是 ________________________________________________。
(3)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是____________________________。
②装置B的作用是_______________________________________________________。
(4)通过上述实验探究过程,可得出装置A中反应的化学方程式是_______________。
(5)①水合肼(N2H4·H2O)是一种重要的化工原料,在医药、农业及燃料上都有着广泛的应用。目前,我国生产水合肼均采用尿素法,即利用NaClO溶液、NaOH溶液与尿素[CO(NH2)2]反应制得粗肼(N2H4)。生成粗肼反应的化学方程式为_______________。
②火箭发射时可用肼(N2H4)为燃料,二氧化氮作氧化剂,生成无毒害的物质,写出反应方程式 _______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个密闭容器,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当左边充入 1mol N2, 右边充入 CO 和 CO2 的混合气体共 8g 时,隔板处于如图位置(保持温度不变),下列说法正确的是
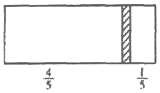
A. 右边 CO 与 CO2 分子数之比为 1:3
B. 右侧 CO 的质量为 2.75g
C. 若改变右边 CO 和 CO2 的充入量而使隔板处于离右端1/6处, 保持温度不变,则前后两次充入容器内的气体压强之比为 5: 3
D. 右侧气体密度是相同条件下氢气密度的 16 倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体物质X中可能含有Fe、Fe2O3、CuO、KCl和Na2CO3中的若干种,为确定其组成,取物质X做如下实验。下列说法正确的是:

A. 固体N可能是Fe、Cu的混合物
B. 溶液Z一定含有KCl和Na2CO3
C. 物质X中一定含有Fe、CuO、Na2CO3
D. 向溶液M中加入KSCN溶液,若溶液不变红,说明物质X中不含Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关苯的性质描述中,正确的是( )
A.苯能使酸性高锰酸钾溶液褪色
B.苯与稀硝酸、稀硫酸混合加热,生成硝基苯
C.苯与溴水混合振荡,静置,下层液体几乎为无色
D.1 mol苯与2 mol氢气发生加成反应生成1 mol环己烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com