高铁酸钾(K
2FeO
4)是一种新型、高效、多功能绿色水处理剂,比Cl
2、O
2、ClO
2、KMnO
4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出.
(1)干法制备高铁酸钠的主要反应为:2FeSO
4+6Na
2O
2═2Na
2FeO
4+2Na
2O+2Na
2SO
4+O
2↑
①该反应中的氧化剂是
Na2O2
Na2O2
,还原剂是
FeSO4和Na2O2
FeSO4和Na2O2
,每生成1molNa
2FeO
4转移
5
5
mol电子
②简要说明K
2FeO
4,作为水处理剂时,在水处理过程中所起的作用
高铁酸钾具有强氧化性,能杀菌消毒,且消毒过程中自身被还原成铁离子,铁离子水解氢氧化铁胶体能吸附除去水中的悬浮杂质
高铁酸钾具有强氧化性,能杀菌消毒,且消毒过程中自身被还原成铁离子,铁离子水解氢氧化铁胶体能吸附除去水中的悬浮杂质
.
(2)湿法制备高铁酸钾(K
2FeO
4)的反应体系中有六种数粒:Fe(OH)
3、ClO
-、OH
-、FeO
42-、Cl
-、H
2O.
①写出并配平湿法制高铁酸钾的离子反应方程式:
2Fe(OH)3+3ClO-+4OH-═2FeO42-+3Cl-+5H2O
2Fe(OH)3+3ClO-+4OH-═2FeO42-+3Cl-+5H2O
.
②每生成1molFeO
42-转移
3
3
mol电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为
0.15
0.15
mol.
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K
2FeO
4),说明什么问题
该温度下高铁酸钾的溶解度比高铁酸钠的溶解度小
该温度下高铁酸钾的溶解度比高铁酸钠的溶解度小
.



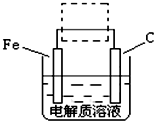 (FeSO4?7H2O)一起净水,其原理为
(FeSO4?7H2O)一起净水,其原理为 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH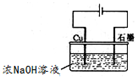 溶液的pH为
溶液的pH为