
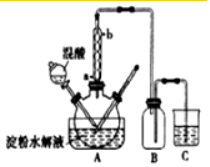
分析 (1)根据浓硫酸的三大特性结合反应解答;
(2)碘水遇到淀粉会变蓝,如果溶液中无淀粉,加入碘水没有变化;
(3)冷凝效果逆流效果好;
(4)装置B的作用是防止发生装置和吸收装置间发生倒吸;
(5)浓硫酸溶于水放热;草酸具有还原性,硝酸能进一步氧化C6H12O6和H2C2O4;
(6)当尾气中n(NO2):n(NO)=1:1时,过量的NaOH溶液能将氮氧化物全部吸收,只生成一种钠盐为亚硝酸钠,优点:提高HNO3利用率(或循环使用氮氧化物); 缺点:NOx(或氮氧化物)吸收不完全;
(7)高锰酸钾为紫红色,过程中不需要加指示剂;在酸性条件下,高锰酸根离子能和草酸发生氧化还原反应生成二价锰离子、二氧化碳和水,根据反应计算.
解答 解:(1)浓硫酸具有强氧化性、吸水性和脱水性,本题实验是将C6H12O6用硝酸氧化可以制备草酸,浓硫酸作催化剂且浓硫酸吸水有利于向生成草酸的方向移动,
故答案为:催化剂的作用;
(2)淀粉遇碘变蓝色,在已经水解的淀粉溶液中滴加几滴碘液,溶液显蓝色,则证明淀粉没有完全水解;溶液若不显色,则证明淀粉完全水解,
故答案为:碘水;
(3)冷凝效果逆流效果好,冷凝水的进口是a进b出,故答案为:a;
(4)装置B的作用是防止发生装置和吸收装置间发生倒吸,起到安全瓶的作用,故答案为:作安全瓶;
(5)混酸为65%HNO3与98%H2SO4的混合液,混合液溶于水放热,温度高能加快化学反应,硝酸能进一步氧化H2C2O4成二氧化碳,
故答案为:硝酸浓度过大.导致葡萄糖被氧化为C〇2,且H2C2O4进一步被氧化;
(6)当尾气中n(NO2):n(NO)=1:1时,过量的NaOH溶液能将氮氧化物全部吸收,只生成一种钠盐为亚硝酸钠,反应的化学方程式为:NO2+NO+2NaOH=2NaNO2+H2O,用含硫酸的母液来吸收氮氧化物,会生成硝酸而重复使用,提高HNO3利用率;但也会造成吸收不充分,造成环境污染,
故答案为:NO2+NO+2NaOH=2NaNO2+H2O;提高HNO3利用率;NOx(或氮氧化物)吸收不完全;
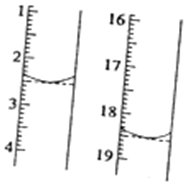
(7)高锰酸钾溶液为紫红色,当达到滴定终点时,再滴入高锰酸钾溶液时,淡紫色不再褪去半分钟内不变化,草酸钠(Na2C2O4)溶于稀硫酸中,然后用酸性高锰酸钾溶液进行滴定,离子方程式为2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O,图示滴定管消耗溶液体积=18.50mL-2.50mL=16.00mL,
n(KMnO4)=0.016L×0.0200mol•L-1=3.2×10-4mol,根据方程式可得:
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
2 5
3.2×10-4mol 8×10-4mol
样品中二水合草酸的质量为m=8×10-4mol×126g/mol=8×126×10-4g=0.1008g,
则该草酸晶体样品中二水合草酸的质量分数为$\frac{0.1008g}{0.12g}$×100%=84.0%,
故答案为:84.0%.
点评 本题主要考查了草酸的制取实验,注意把握实验的原理,熟练进行氧化还原计算是解答的关键,要求具备一定的理论分析能力和计算解决问题的能力,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | m=2 | |
| B. | 两次平衡的平衡常数相同 | |
| C. | X与Y平衡转化率之比为1:1 | |
| D. | 第二次平衡时,Z的浓度为0.4mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
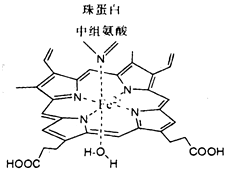 红细胞中血红素结构如图所示,回答下列问题:
红细胞中血红素结构如图所示,回答下列问题: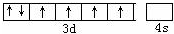 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径:W>Z | |
| B. | X和W形成的化合物属于离子化合物 | |
| C. | 由X、Y、Z三种元素组成化合物的水溶液一定显酸性 | |
| D. | Z最简单氢化物分子间存在氢键,故其稳定性强于Y最简单氢化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 将FeCl3溶液加入Mg(OH)2悬浊液中 | 观察到沉淀由白色变为红褐色 | Fe(OH)3的溶解度大于Mg(OH)2 |
| B | 向某溶液中滴加BaCl2溶液,随后加稀硝酸酸化 | 溶液中产生白色沉淀,加稀硝酸不溶解 | 原溶液中一定含有SO42- |
| C | 将稀硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中 | 溶液变黄色 | 氧化性:H2O2比Fe3+强 |
| D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 燃烧法是测定有机化合物化学式的一种重要方法.现完全燃烧一定质量的某烃,燃烧产物依次通过如图所示的装置,实验结束后,称得甲装置增重3.6g,乙装置增重8.8g,又知该烃的蒸汽密度是同温同压下氢气密度的28倍.
燃烧法是测定有机化合物化学式的一种重要方法.现完全燃烧一定质量的某烃,燃烧产物依次通过如图所示的装置,实验结束后,称得甲装置增重3.6g,乙装置增重8.8g,又知该烃的蒸汽密度是同温同压下氢气密度的28倍.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com