
 .
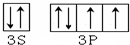
. 分析 质量数为32,核内有16个中子的原子,则质子数为32-16=16,为S元素的原子,核外有16个电子,未成对电子优先单独占据一个轨道自旋方向相同,根据构造原理写出电子排布式,主族元素价电子为最外层电子,画出价电子轨道排布图,以此来解答.
解答 解:质量数为32,核内有16个中子的原子,则质子数为32-16=16,为S元素的原子,其电子排布式为1s22s22p63s23p4,S原子最外层6个电子,为3s23p4,3p轨道中4个电子,且有2个单电子,其价电子轨道排布图为 ,
,
故答案为:1s22s22p63s23p4; .
.
点评 本题考查了电子排布式和电子排布图,为高频考点,把握质子数的计算及电子排布规律为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.1s | B. | 2.5s | C. | 5s | D. | 10s |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
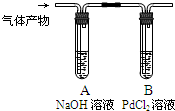 黑火药爆炸时发生多种化学反应,其中主要化学反应方程式为:
黑火药爆炸时发生多种化学反应,其中主要化学反应方程式为: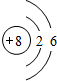 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微粒半径大小:S2->Cl->F->Na+>Al3+ | |
| B. | 热稳定性大小:SiH4<PH3<NH3<H2O<HF | |
| C. | 熔点高低:金刚石>石墨>食盐>干冰>碘晶体 | |
| D. | 沸点高低:NH3>AsH3>PH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
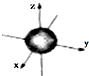
| A. | 3d3表示3d能级上有3个轨道 | |
| B. | ns能级的原子轨道图都可以用右图表示 | |
| C. | 1s电子云呈球形,表示电子绕原子核做圆周运动 | |
| D. | 电子云图的黑点密度越大,说明核外空间电子数越多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
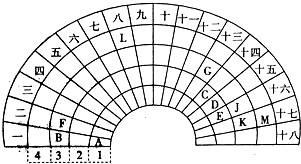
 .
. ,用电子式表示FM2的形成过程
,用电子式表示FM2的形成过程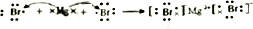 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
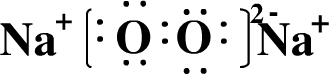 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCHO | B. | CH3COOCH2CH3 | C. | HOOCCOOH | D. | CH3COOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com