
·ÖĪö £Ø1£©øł¾Ż·½³ĢŹ½ÖŖ£¬Čē¹ūÉś³É6molC£¬ŌņĻūŗÄn£ØA£©=$\frac{1}{2}$n£ØC£©£¬·“Ó¦³õŹ¼a=n£ØA£©£ØŹ£Óą£©+n£ØA£©£Ø·“Ó¦£©£»
£Ø2£©¢Ł»ģŗĻĘųĢåÖŠn£ØC£©=32mol”Į25%=8mol£¬v£ØC£©=$\frac{\frac{”÷n}{V}}{”÷t}$£»
¢ŚĻČ¼ĘĖćĘ½ŗāŹ±n£ØA£©£¬ŌŁøł¾Żc=$\frac{n}{V}$¼ĘĖćc£ØA£©£»
£Ø3£©ĻČ¼ĘĖćbÖµ£¬ŌŁ¼ĘĖćŌ»ģŗĻĘųĢåÓėĘ½ŗā»ģŗĻĘųĢåµÄ×ÜĪļÖŹµÄĮæÖ®±Č£®
½ā“š ½ā£ŗ£Ø1£©øł¾Ż·½³ĢŹ½ÖŖ£¬Čē¹ūÉś³É6molC£¬ŌņĻūŗÄn£ØA£©=$\frac{1}{2}$n£ØC£©=$\frac{1}{2}$”Į6mol=3mol£¬·“Ó¦³õŹ¼a=n£ØA£©£ØŹ£Óą£©+n£ØA£©£Ø·“Ó¦£©=13mol+3mol=16mol£¬
“š£ŗaĪŖ16£»
£Ø2£©¢Ł»ģŗĻĘųĢåÖŠn£ØC£©=32mol”Į25%=8mol£¬v£ØC£©=$\frac{\frac{”÷n}{V}}{”÷t}$=$\frac{\frac{8mol}{2L}}{5min}$=0.8mol/£ØL£®min£©£¬
“š£ŗCµÄ·“Ó¦ĖŁĀŹĪŖ0.8mol/£ØL£®min£©£»
¢Śøł¾Ż·½³ĢŹ½ÖŖ£¬Ę½ŗāŹ±Éś³É8molC£¬ŌņĻūŗÄn£ØA£©=$\frac{1}{2}$n£ØC£©=$\frac{1}{2}$”Į8mol=4mol£¬Ź£Óąn£ØA£©=16mol-4mol=12mol£¬Ę½ŗāŹ±c£ØA£©=$\frac{n}{V}$=$\frac{12mol}{2L}$=6mol/L£¬
“š£ŗ5minŗóČŻĘ÷ÖŠAµÄĪļÖŹµÄĮæÅØ¶ČŹĒ6mol/L£»
£Ø3£©N2””””+3H2””?2NH3””””””””””””””””£¬
æŖŹ¼£Ømol£©16””””b”””””””””” 0
±ä»Æ£Ømol£©4””””12”””””””””” 8
Ę½ŗā£Ømol£©12””£Øb-12£©8
$\frac{8mol}{£Ø12+b-12+8£©mol}”Į$100%=25%£¬
b=24£¬
Ō»ģŗĻĘųĢåÓėĘ½ŗā»ģŗĻĘųĢåµÄ×ÜĪļÖŹµÄĮæÖ®±Č=£Ø16+24£©mol£ŗ32mol=5£ŗ4£¬
“š£ŗŌ»ģŗĻĘųĢåÓėĘ½ŗā»ģŗĻĘųĢåµÄ×ÜĪļÖŹµÄĮæÖ®±ČnŹ¼£ŗnĘ½=5£ŗ4£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗā¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬²ąÖŲæ¼²éѧɜ·ÖĪö¼ĘĖćÄÜĮ¦£¬ĄūÓĆČż¶ĪŹ½·Ø·ÖĪö½ā“š¼“æÉ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
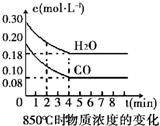
| Ź±¼ä£Ømin£© | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
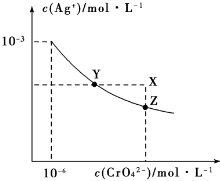 t”ꏱAg2CrO4ŌŚĖ®ÖŠµÄ³ĮµķČܽāĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
t”ꏱAg2CrO4ŌŚĖ®ÖŠµÄ³ĮµķČܽāĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ¼ÓČČÕō·¢±„ŗĶAg2CrO4ČÜŅŗŌŁ»Öø“µ½t”ę£¬æÉŹ¹ČÜŅŗÓÉYµć±äµ½Zµć | |
| B£® | ŌŚXµćƻӊAg2CrO4³ĮµķÉś³É£¬Ōņ“ĖŹ±ĪĀ¶ČµĶÓŚt”ę | |
| C£® | Ļņ±„ŗĶAg2CrO4ČÜŅŗÖŠ¼ÓČėÉŁĮæAgNO3¹ĢĢ壬æÉŹ¹ČÜŅŗÓÉZµćµ½Yµć | |
| D£® | ŌŚt”ꏱ£¬Ag2CrO4µÄKspĪŖ1”Į10-9 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
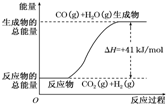 £Ø1£©ŅŃÖŖ14g N2Óė×ćĮæH2·“Ó¦·Å³ö46kJµÄČČĮ棬ŌņøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ŹĒN2£Øg£©+3H2£Øg£©?2NH3£Øg£©£»”÷H=-92.4kJ/mol
£Ø1£©ŅŃÖŖ14g N2Óė×ćĮæH2·“Ó¦·Å³ö46kJµÄČČĮ棬ŌņøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ŹĒN2£Øg£©+3H2£Øg£©?2NH3£Øg£©£»”÷H=-92.4kJ/mol ”ś
”ś
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ü | B£® | ¢Ł¢Ü¢Ż | C£® | ¢Ł¢Ś¢Ū¢Ü | D£® | ¢Ś¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀ£¬AgClČōŅŖŌŚNaIČÜŅŗÖŠæŖŹ¼×Ŗ»ÆĪŖAgI£¬ŌņNaIµÄÅØ¶Č±ŲŠė²»µĶÓŚ$\frac{1}{\sqrt{1.8}}$”Į10-11 mol•L-1 | |
| B£® | ĻņBaCl2ČÜŅŗÖŠ¼ÓČėAgNO3ŗĶKI£¬µ±Į½ÖÖ³Įµķ¹²“ꏱ£¬$\frac{c£Ø{I}^{-}£©}{c£ØC{l}^{-}£©}$=5.6”Į10-7 | |
| C£® | AgI±ČAgCløüÄŃČÜÓŚĖ®£¬ĖłŅŌ£¬AgClæÉŅŌ×Ŗ»ÆĪŖAgI | |
| D£® | AgCl²»ČÜÓŚĖ®£¬²»ÄÜ×Ŗ»ÆĪŖAgI |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2O2µÄµē×ÓŹ½£ŗ | B£® | ClŌ×ӵĽį¹¹Ź¾ŅāĶ¼£ŗ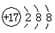 | ||
| C£® | HClO·Ö×ӵĽį¹¹Ź½£ŗH-Cl-O | D£® | ŅŅĻ©µÄ½į¹¹¼ņŹ½£ŗCH2CH2 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com