
 ,含有的化学键类型有离子键、共价键
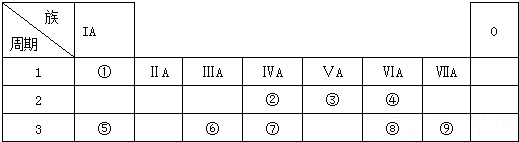
,含有的化学键类型有离子键、共价键分析 由元素在周期表中的位置,可知①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,⑧是S,⑨是Cl.
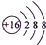
(1)同周期自左而右金属性减弱、同主族自上而下金属性增强;硫离子核外有3个电子层,各层电子数为2、8、8;
(2)同周期自左而右原子半径减小、同主族自上而下原子半径增大;
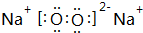
(3)④、⑤形成的一种化合物是淡黄色固体为Na2O2,由钠离子与过氧根离子构成;
(4)利用最高价含氧酸的酸性强弱比较,即利用强酸制备弱酸;
(5)a.金属性越强,最高价氧化物对应水化物的碱性越强;
b.水分子之间存在氢键,沸点高于硫化氢;
c.应是最高价含氧酸的酸性③强于②;
d.冰分子之间形成氢键,每个水分子与周围的4个水分子形成四面体结构,冰晶体中水分子之间有相当大的空间,空间利用率低;
(6)化合物A由元素④和⑨组成,相同条件下,气态A相对空气的密度为3,则Mr(A)=29×3=87,A中元素④的质量分数为约为18.4%,则O原子数目为$\frac{87×18.4%}{16}$=1,Cl原子数目为$\frac{87-16}{35.5}$=2,故A的化学式为Cl2O,A与NH3反应,生成一种离子化合物B、气体单质C和一种常见液体D,C为空气的主要成分,则B为NH4Cl、C为N2、D为H2O.
解答 解:由元素在周期表中的位置,可知①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,⑧是S,⑨是Cl.
(1)同周期自左而右金属性减弱、同主族自上而下金属性增强,故上述元素中Na的金属性最强;硫离子核外有3个电子层,各层电子数为2、8、8,离子结构示意图为 ,
,
故答案为:Na; ;
;
(2)同周期自左而右原子半径减小、同主族自上而下原子半径增大,故原子半径:Na>Al>O,
故答案为:Na>Al>O;
(3)④、⑤形成的一种化合物是淡黄色固体为Na2O2,由钠离子与过氧根离子构成,电子式为 ,含有离子键、共价键,
,含有离子键、共价键,
故答案为: ;离子键、共价键;
;离子键、共价键;
(4)利用最高价含氧酸的酸性强弱比较,即利用强酸制备弱酸,反应方程式为:Na2SiO3+H2O+CO2=H2SiO3↓+Na2CO3,
故答案为:Na2SiO3+H2O+CO2=H2SiO3↓+Na2CO3;
(5)a.金属性Na>Al,金属性越强,最高价氧化物对应水化物的碱性越强,故碱性氢氧化钠>氢氧化铝,故a正确;
b.共价键影响其稳定性,水分子之间存在氢键,沸点高于硫化氢,故b错误;
c.应是最高价含氧酸的酸性③强于②,故c错误;
d.冰分子之间形成氢键,每个水分子与周围的4个水分子形成四面体结构,冰晶体中水分子之间有相当大的空间,空间利用率低,固态时的密度小于液态时密度,故d正确,
故选:ad;
(6)化合物A由元素④和⑨组成,相同条件下,气态A相对空气的密度为3,则Mr(A)=29×3=87,A中元素④的质量分数为约为18.4%,则O原子数目为$\frac{87×18.4%}{16}$=1,Cl原子数目为$\frac{87-16}{35.5}$=2,故A的化学式为Cl2O,A与NH3反应,生成一种离子化合物B、气体单质C和一种常见液体D,C为空气的主要成分,则B为NH4Cl
、C为N2、D为H2O,反应方程式为:3Cl2O+10NH3=6NH4Cl+2N2+3H2O,
故答案为:Cl2O;3Cl2O+10NH3=6NH4Cl+2N2+3H2O.
点评 本题考查元素周期表与元素周期律的综合应用,是对学生综合能力的考查,需要学生具备扎实的基础,难度中等.


 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子晶体中的各相邻原子都以共价键相结合 | |
| B. | 金属导电的原因是在外电场作用下金属产生自由电子,电子定向运动 | |
| C. | 分子晶体的熔沸点很低,常温下都呈液态或气态 | |
| D. | 离子晶体中每个离子周围均吸引着6个带相反电荷的离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用反应物A表示该反应的反应速率为0.6 mol•L-1•min-1 | |
| B. | 用反应物B表示该反应的反应速率为1.8 mol•L-1•min-1 | |
| C. | 反应达到平衡时$\frac{2}{3}$v(B)正=v(C)逆 | |
| D. | 升高温度可加快正反应的速率,同时降低逆反应的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 溴苯是一种化工原料,实验室用以下甲、乙、丙、丁等仪器组合,合成溴苯的装置示意图(其余辅助仪器略去)及有关数据如下,按要求回答下列问题:
溴苯是一种化工原料,实验室用以下甲、乙、丙、丁等仪器组合,合成溴苯的装置示意图(其余辅助仪器略去)及有关数据如下,按要求回答下列问题:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/°C | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、NH4+、OH-、SO42- | B. | H+、Fe2+、SO42-、ClO- | ||
| C. | Na+、Ca2+、Cl-、CO32- | D. | K+、Ca2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(NH3)=0.3 mol/(L•min) | B. | v(N2)=0.01 mol/(L•s) | ||
| C. | v(N2)=0.2 mol/(L•min) | D. | v(H2)=0.3 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放热反应 | B. | 吸热反应 | C. | 氧化还原反应 | D. | 可逆反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com