

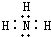 ���ʴ�Ϊ��
���ʴ�Ϊ��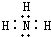 ��
��
| ||
| ���� |
| ||
| ���� |
| 2 |
| 3 |
| 2 |
| 3 |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ԫ�����ڱ����߸����� |
| B��Ԫ�����ڱ���18���� |
| C��IA���Ԫ��ȫ���ǽ���Ԫ�� |
| D����������ָ��һ���������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
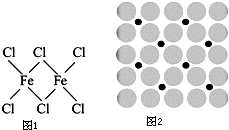 �������Ļ��������������������й㷺Ӧ�ã���ش��������⣺
�������Ļ��������������������й㷺Ӧ�ã���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A | |||||||||||||||||
| B | C | ||||||||||||||||
| D | E | ||||||||||||||||

| Ԫ�� | D | E | |
| ������ /kJ?mol-1 |
I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��������ij���������ϵĻ���ԭ��֮һ����C��H��O����Ԫ����ɣ�����ӽṹģ����ͼ��ʾ��ͼ��������֮�����ߴ�����ѧ��������˫���������ݷ��ӽṹģ��
��������ij���������ϵĻ���ԭ��֮һ����C��H��O����Ԫ����ɣ�����ӽṹģ����ͼ��ʾ��ͼ��������֮�����ߴ�����ѧ��������˫���������ݷ��ӽṹģ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��װ���г��ڢٴ������������������ڢڴ������������� | ||||
B��װ���з�����Ӧ�����ӷ���ʽΪ��2Cl-+2H+
| ||||
| C����װ���ǽ�����ת��Ϊ��ѧ�� | ||||
| D�������ӽ���Ĥֻ����������ͨ����������������ͨ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������е�Ԫ�ػ��ϼ۶�Ϊ-3�� |
| B��������ȷų����� |
| C��������ξ��ֽܷ� |
| D������о��������Ӽ����ۼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��XԪ�������ڱ��е�λ��ֻ���ǵ�2���ڢ�A�� |
| B����X�ij�����������Xn-�ܸ�Y�ĵ��ʷ���������ԭ��Ӧ�û���X����˵��Y�ķǽ����Ա�X���� |
| C����Y�ķǽ����Ա�X��ǿ������ͬһ�ֻ�ԭ����Ӧʱ��һ��Yԭ�ӵõ��ĵ�����һ����һ��Xԭ�ӵõ��ĵ������� |
| D����X���γ�XO32-��XO42-��X2O32-��Y���γ�YO3-��YO4-����X��Yһ����ͬһ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1mol/L Na2CO3��Һ�У�c��Na+��+c��H+��=c��CO32-��+c��HCO3-��+c��OH-�� |
| B��0.1mol/L ��NH4��2SO4��Һ�У�c��SO42-����c��NH4+����c��H+����c��OH-�� |
| C��0.1mol/L NaHCO3��Һ�У�c��OH-��=2c��H2CO3��+c��HCO3-��+c��H+�� |
| D��0.1mol/L Na2S��Һ�У�c��Na+��=2c��S2-��+2c��HS-��+2c��H2S�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com