
”¾ĢāÄæ”æĻņÄ³ČŻ»żŅ»¶ØµÄĆܱÕČŻĘ÷ÖŠ³äČė2molSO2ŗĶ1molO2£¬Ņ»¶ØĢõ¼žĻĀ·¢ÉśČēĻĀ·“Ó¦:2SO2+O2![]() 2SO3”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
2SO3”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. ÉżøßĪĀ¶Č»ņ³äČėŅ»¶ØĮæO2¾łÄܼÓæģ»Æѧ·“Ó¦ĖŁĀŹ
B. “ļµ½Ę½ŗāדĢ¬Ź±£¬SO2”¢O2”¢SO3ĪļÖŹµÄĮæÖ®±ČŅ»¶ØĪŖ2:1:2
C. µ±SO2µÄÉś³ÉĖŁĀŹÓėSO3µÄÉś³ÉĖŁĀŹĻąµČŹ±£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬
D. “ļµ½Ę½ŗāדĢ¬Ź±£¬Éś³ÉSO3µÄĪļÖŹµÄĮæŅ»¶ØŠ”ÓŚ2mol
”¾“š°ø”æB
”¾½āĪö”æøł¾ŻÓ°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄŅņĖŲŗĶ»Æѧ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāµÄ±źÖ¾½ųŠŠ½ā“š”£Ōö¼Ó·“Ó¦ÅØ¶Č»ņÉś³ÉĪļµÄÅØ¶Č»Æѧ·“Ó¦ĖŁĀŹ¼Óæģ£»ÉżøßĪĀ¶Č»Æѧ·“Ó¦ĖŁĀŹ¼Óæģ£»»ÆŃ§Ę½ŗāµÄ±źÖ¾ŹĒø÷ĪļÖŹµÄÅØ¶Č²»ŌŚøÄ±ä£¬Õż·“Ó¦ĖŁĀŹµČÓŚÄę·“Ó¦ĖŁĀŹ”£
A.øł¾ŻÓ°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄŅņĖŲÖŖ·“Ó¦2SO2+O2![]() 2SO3£¬Čē¹ūÉżøßĪĀ¶Č»ņ³äČėŅ»¶ØĮæO2¾łÄܼÓæģ»Æѧ·“Ó¦ĖŁĀŹ£¬¹ŹAÕżČ·£»B. ³õŹ¼¼ÓČė2molSO2ŗĶ1molO2£¬øł¾Ż·“Ó¦2SO2+O2
2SO3£¬Čē¹ūÉżøßĪĀ¶Č»ņ³äČėŅ»¶ØĮæO2¾łÄܼÓæģ»Æѧ·“Ó¦ĖŁĀŹ£¬¹ŹAÕżČ·£»B. ³õŹ¼¼ÓČė2molSO2ŗĶ1molO2£¬øł¾Ż·“Ó¦2SO2+O2![]() 2SO3£¬ŅņĪŖŹĒæÉÄę·“Ó¦²»ÄܽųŠŠ³¹µ×£¬ĖłŅŌ“ļµ½Ę½ŗāדĢ¬Ź±£¬SO2”¢O2”¢SO3ĪļÖŹµÄĮæÖ®±Č²»Ņ»¶ØĪŖ2:1:2£¬¹ŹB“ķĪó£»C. µ±SO2µÄÉś³ÉĖŁĀŹÓėSO3µÄÉś³ÉĖŁĀŹĻąµČŹ±£¬ĖµĆ÷ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬¹ŹCÕżČ·£»D.ŅņĪŖ2SO2+O2
2SO3£¬ŅņĪŖŹĒæÉÄę·“Ó¦²»ÄܽųŠŠ³¹µ×£¬ĖłŅŌ“ļµ½Ę½ŗāדĢ¬Ź±£¬SO2”¢O2”¢SO3ĪļÖŹµÄĮæÖ®±Č²»Ņ»¶ØĪŖ2:1:2£¬¹ŹB“ķĪó£»C. µ±SO2µÄÉś³ÉĖŁĀŹÓėSO3µÄÉś³ÉĖŁĀŹĻąµČŹ±£¬ĖµĆ÷ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬¹ŹCÕżČ·£»D.ŅņĪŖ2SO2+O2![]() 2SO3ŹĒæÉÄę·“Ó¦²»ÄܽųŠŠ³¹µ×£¬“ļµ½Ę½ŗāדĢ¬Ź±£¬Éś³ÉSO3µÄĪļÖŹµÄĮæŅ»¶ØŠ”ÓŚ2mol£¬¹ŹDÕżČ·£»“š°ø£ŗŃ”B”£
2SO3ŹĒæÉÄę·“Ó¦²»ÄܽųŠŠ³¹µ×£¬“ļµ½Ę½ŗāדĢ¬Ź±£¬Éś³ÉSO3µÄĪļÖŹµÄĮæŅ»¶ØŠ”ÓŚ2mol£¬¹ŹDÕżČ·£»“š°ø£ŗŃ”B”£


 ×÷Ņµøص¼ĻµĮŠ“š°ø
×÷Ņµøص¼ĻµĮŠ“š°ø Ķ¬²½Ń§µäŅ»æĪ¶ąĮ·ĻµĮŠ“š°ø
Ķ¬²½Ń§µäŅ»æĪ¶ąĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķŹĒŌŖĖŲÖÜĘŚ±ķµÄ¶ĢÖÜĘŚ²æ·Ö£¬±ķÖŠ×ÖÄø·Ö±š±ķŹ¾Ņ»ÖÖŌŖĖŲ”£

Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ÓɱķÖŠĮ½ÖÖŌŖĖŲµÄŌ×Ó°“1”Ć1×é³ÉµÄ³£¼ūŅŗĢ¬»ÆŗĻĪļµÄĻ”ČÜŅŗŅ×±»“߻Ʒֽā£¬æÉŹ¹ÓĆµÄ“ß»Æ¼ĮĪŖ(ĢīŠņŗÅ)____”£
a.MnO2 b.NaCl c.Na2SO3 d.KMnO4
£Ø2£©d”¢e”¢hĖÄÖÖŌŖĖŲ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļµÄĖįŠŌÓÉČõµ½ĒæµÄĖ³ŠņĪŖ£ØÓĆ»ÆѧŹ½±ķŹ¾£©________”£b”¢c”¢f”¢g”¢hŠĪ³ÉµÄ¼ņµ„Ąė×ӵİė¾¶ÓÉŠ”µ½“óµÄĖ³ŠņĪŖ_______(ÓĆĄė×Ó·ūŗÅĢīŠ“)”£
£Ø3£©ŌŚ1LµÄĆܱÕČŻĘ÷ÖŠ£¬ĶØČė1molf2ĘųĢåŗĶ3mola2ĘųĢ壬Ņ»¶ØĪĀ¶ČĻĀ·“Ӧɜ³Éfa3ĘųĢ壬2minŹ±£¬²āµĆf2µÄÅضČĪŖ0.75mol”¤L-1£¬Ōņ2minŹ±fa3µÄĪļÖŹµÄĮæĪŖ_____mol£»·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬ČōŌö“ófa3µÄ²śĀŹ£¬æÉŅŌ²ÉČ”“ėŹ©£ØĢīŠņŗÅ£©_____”£
¢ŁÉżøßĪĀ¶Č ¢ŚŗćČŻ³äČėŗ¤Ęų
¢ŪĻņĆܱÕČŻĘ÷ÄŚ³äČėf2Ęų ¢Ü¼°Ź±·ÖĄė³öfa3ĘųĢå
£Ø4£©dÓėaæÉŠĪ³É»ÆŗĻĪļd5a12£¬ŹŌŠ“³öĖüµÄŅ»ĀČČ”“śĪļÓŠŅ»ÖÖµÄĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½_____”£
£Ø5£©a”¢dĮ½ÖÖŌŖĖŲæÉŠĪ³É¶ąÖÖ»ÆŗĻĪļ£¬ĘäÖŠ»ÆŗĻĪļXµÄ²śĮæŹĒŗāĮæŅ»øö¹ś¼ŅŹÆÓĶ»Æ¹¤·¢Õ¹Ė®Ę½µÄ±źÖ¾”£XæÉÓėH2OŌŚŅ»¶ØĢõ¼žĻĀ·“Ӧɜ³É»ÆŗĻĪļŅŅ“¼£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ_______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æX”¢Y”¢Z”¢WĪŖĒ°20ŗÅŌ×ÓŠņŹżŅĄ“ĪµŻŌöµÄĖÄÖÖŌŖĖŲ£¬XÓėYÄÜŠĪ³É![]() ŗĶ
ŗĶ![]() Į½ÖÖ³£ĪĀĻĀ³ŹŅŗĢ¬µÄ»ÆŗĻĪļ£¬ZŌ×ÓµÄŌ×ÓŠņŹżĪŖ×īĶā²ćµē×ÓŹżµÄ3±¶£¬µČĪļÖŹµÄĮæµÄµ„ÖŹWĖłŗ¬µē×ÓŹżĪŖ»ÆŗĻĪļ
Į½ÖÖ³£ĪĀĻĀ³ŹŅŗĢ¬µÄ»ÆŗĻĪļ£¬ZŌ×ÓµÄŌ×ÓŠņŹżĪŖ×īĶā²ćµē×ÓŹżµÄ3±¶£¬µČĪļÖŹµÄĮæµÄµ„ÖŹWĖłŗ¬µē×ÓŹżĪŖ»ÆŗĻĪļ![]() µē×ÓŹżµÄĮ½±¶£¬ŌņŅŌĻĀĖµ·Ø“ķĪóµÄŹĒ
µē×ÓŹżµÄĮ½±¶£¬ŌņŅŌĻĀĖµ·Ø“ķĪóµÄŹĒ
A. Ēā»ÆĪļµÄĪČ¶ØŠŌĪŖ![]()
B. ![]() µÄµē×ÓŹ½ĪŖ
µÄµē×ÓŹ½ĪŖ![]()
C. ![]() ÖŠ¼Čŗ¬ÓŠ¹²¼Ū¼üÓÖŗ¬ÓŠĄė×Ó¼ü
ÖŠ¼Čŗ¬ÓŠ¹²¼Ū¼üÓÖŗ¬ÓŠĄė×Ó¼ü
D. ![]() ÄÜÓė
ÄÜÓė![]() ·“Ӧɜ³É
·“Ӧɜ³É![]()
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ“ÓĆŗŗĶŹÆÓĶÖŠæÉŅŌĢįĮ¶³ö»Æ¹¤ŌĮĻAŗĶB£¬AŹĒŅ»ÖÖ¹ūŹµ“ߏģ¼Į£¬ĖüµÄ²śĮæÓĆĄ“ŗāĮæŅ»øö¹ś¼ŅµÄŹÆÓĶ»Æ¹¤·¢Õ¹Ė®Ę½£®BŹĒŅ»ÖÖ±ČĖ®ĒįµÄÓĶדŅŗĢ壬B½öÓÉĢ¼ĒāĮ½ÖÖŌŖĖŲ×é³É£¬Ģ¼ŌŖĖŲÓėĒāŌŖĖŲµÄÖŹĮæ±ČĪŖ12£ŗ1£¬BµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ78£®»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©AµÄµē×ÓŹ½ ______________ £¬AµÄ½į¹¹¼ņŹ½ _______________ £®
£Ø2£©ÓėAĻąĮŚµÄĶ¬ĻµĪļCŹ¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ«µÄ»Æѧ·“Ó¦·½³ĢŹ½ ______________________£¬·“Ó¦ĄąŠĶ_______________”£
£Ø3£©ŌŚµāĖ®ÖŠ¼ÓČėBÕńµ“¾²ÖĆŗóµÄĻÖĻó_________________________
£Ø4£©BÓėÅØH2SO4ÓėÅØHNO3ŌŚ50-60”ę·“Ó¦µÄ»Æѧ·“Ó¦·½³ĢŹ½ ________________________£¬·“Ó¦ĄąŠĶ______________________”£
£Ø5£©µČÖŹĮæµÄA”¢BĶźČ«Č¼ÉÕŹ±ĻūŗÄO2µÄĪļÖŹµÄĮæ______£ØĢī”°A£¾B”±»ņ”°A£¼B”±»ņ”°A=B”±£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
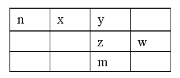
”¾ĢāÄæ”æx”¢y”¢z”¢w”¢nĪŖĪåÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäÖŠYŌŖĖŲŌ×ÓŗĖĶā×īĶā²ćµē×ÓŹżŹĒĘäµē×Ó²ćŹżµÄ3±¶£¬ĖüĆĒŌŚÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆČēĶ¼ĖłŹ¾£ŗ
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)wĪ»ÓŚÖÜĘŚ±ķÖŠµŚ__________ÖÜĘŚ£¬µŚ__________×唣
(2)n”¢z”¢w”¢ČżÖÖŌŖĖŲ×īøß¼ŪŃõ»ÆĪļĖ®»ÆĪļµÄĖįŠŌÓÉČõµ½ĒæµÄĖ³ŠņĪŖ£ŗ__________£ØÓĆ»ÆѧŹ½±ķŹ¾£©”£
(3)ĻĀĮŠŹĀŹµÄÜĖµĆ÷yŌŖĖŲµÄ·Ē½šŹōŠŌ±ČzŌŖĖŲµÄ·Ē½šŹōŠŌĒæµÄŹĒ____
A£®yµ„ÖŹÓėzµÄĘųĢ¬Ēā»ÆĪļĖ®ČÜŅŗ·“Ó¦£¬ČÜŅŗ±ä»ė×Ē
B£®ŌŚŃõ»Æ»¹Ō·“Ó¦ÖŠ£¬1molyµ„ÖŹ±Č1molzµĆµē×Ó¶ą
C£®yŗĶzĮ½ŌŖĖŲµÄ¼ņµ„Ēā»ÆĪļŹÜČČ·Ö½ā£¬Ē°ÕߵķֽāĪĀ¶Čøß
D£®yŌŖĖŲ×īøß¼ŪŃõ»ÆĪļĖ®»ÆĪļĖįŠŌ±ČzŌŖĖŲ×īøß¼ŪŃõ»ÆĪļĖ®»ÆĪļĖįŠŌĒæ
(4)yŗĶĒāŌŖĖŲŠĪ³ÉµÄ10µē×ÓĪ¢Į£ÖŠ³£¼ū![]() ¼ŪŃōĄė×ÓĪŖ__________£ØĢī»ÆѧŹ½£©£»zŗĶĒāŌŖĖŲŠĪ³ÉµÄ18µē×ÓĪ¢Į£ÖŠ³£¼ū
¼ŪŃōĄė×ÓĪŖ__________£ØĢī»ÆѧŹ½£©£»zŗĶĒāŌŖĖŲŠĪ³ÉµÄ18µē×ÓĪ¢Į£ÖŠ³£¼ū![]() ¼ŪŅõĄė×ӵĵē×ÓŹ½ĪŖ__________”£
¼ŪŅõĄė×ӵĵē×ÓŹ½ĪŖ__________”£
(5)»ÆŗĻĪļnyz“ęŌŚÓŚĢģČ»ĘųÖŠ£¬æÉŅŌÓĆNaOHČÜŅŗĻ“µÓ³żČ„”£»ÆŗĻĪļnyzµÄµē×ÓŹ½ĪŖ__________£¬ĘäÓėNaOHČÜŅŗ·“Ó¦³żÉś³ÉĮ½ÖÖÕżŃĪĶā£¬»¹ÓŠĖ®Éś³É£¬Ęä»Æѧ·½³ĢŹ½ĪŖ__________”£
(6)mŌŖĖŲµÄŌ×ÓŠņŹżĪŖ__________£¬ĖüŹĒŅ»ÖÖ__________”££ØĢī”°½šŹō”±»ņ”°·Ē½šŹō”±£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŠ”×éĪŖĢ½¾æ²ŻĖįŃĒĢś(FeC2O4)µÄČČ·Ö½ā²śĪļ£¬°“ĻĀĆęĖłŹ¾×°ÖĆ½ųŠŠŹµŃ锣ŅŌĻĀĖµ·Ø“ķĪóµÄŹĒ
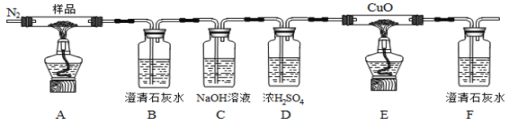
A. ŹµŃéÖŠ¹Ū²ģµ½×°ÖĆB”¢FÖŠŹÆ»ŅĖ®±ä»ė×Ē£¬EÖŠ¹ĢĢå±äĪŖŗģÉ«£¬ŌņÖ¤Ć÷·Ö½ā²śĪļÖŠÓŠCO2ŗĶCOĘųĢå
B. ·“Ó¦½įŹųŗó£¬Č”AÖŠ¹ĢĢåČÜÓŚĻ”ĮņĖį£¬ĻņĘäÖŠµĪ¼Ó1”«2µĪKSCNČÜŅŗ£¬ČÜŅŗĪŽŃÕÉ«±ä»Æ£¬Ö¤Ć÷·Ö½ā²śĪļÖŠ²»ŗ¬Fe2O3
C. ×°ÖĆCµÄ×÷ÓĆŹĒ³żČ„»ģŗĻĘųÖŠµÄCO2
D. ·“Ó¦½įŹųŗó£¬Ó¦ĻØĆšA”¢E“¦¾Ę¾«µĘŗ󣬳֊ųĶØČėN2Ö±ÖĮĪĀ¶Č»Öø“ÖĮŹŅĪĀ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚŅ©Ę·µÄŹ¹ÓĆŗĶ×÷ÓƵÄĖµ·Ø“ķĪóµÄŹĒ(””””)
A.R±ķŹ¾“¦·½Ņ©,OTC±ķŹ¾·Ē“¦·½Ņ©
B.¶¾Ę·¾ĶŹĒÓŠ¶¾µÄŅ©Ę·
C.Į½Ē§ÄźĒ°µÄ”¶ÉńÅ©±¾²Ż¾”·ÖŠ¾ĶÓŠĀé»ĘÄÜ”°Ö¹æČÄęÉĻĘų”±µÄ¼ĒŌŲ
D.Āé»Ę¼īŹĒ¹ś¼Ź°ĀĪÆ»įŃĻøń½ūÖ¹Ź¹ÓƵĊĖ·Ü¼Į
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĢžAŹĒÓŠ»ś»Æѧ¹¤ŅµµÄ»ł±¾ŌĮĻ£¬Ęä²śĮææÉŅŌÓĆĄ“ŗāĮæŅ»øö¹ś¼ŅµÄŹÆÓĶ»Æ¹¤·¢Õ¹Ė®Ę½£¬A»¹ŹĒŅ»ÖÖÖ²ĪļÉś³¤µ÷½Ś¼Į£¬AæÉ·¢ÉśČēĶ¼ĖłŹ¾µÄŅ»ĻµĮŠ»Æѧ·“Ó¦£¬ĘäÖŠ¢Ł¢Ś¢ŪŹōÓŚĶ¬ÖÖ·“Ó¦ĄąŠĶ”£øł¾ŻĶ¼»Ų“šĻĀĮŠĪŹĢā”£
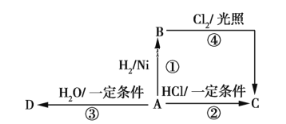
(1)Š“³öA”¢B”¢C”¢DµÄ½į¹¹¼ņŹ½£ŗA_____£¬ B_____£¬C_____£¬ D______”£
(2)Š“³ö¢Ś”¢¢ÜĮ½²½·“Ó¦µÄ»Æѧ·½³ĢŹ½£¬²¢×¢Ć÷·“Ó¦ŠĶ£ŗ
¢Ś___________£¬·“Ó¦ĄąŠĶ________£»
¢Ü___________£¬·“Ó¦ĄąŠĶ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£ØĢāĪÄ£©»ÆŗĻĪļN¾ßÓŠÕņĶ“”¢ĻūŃ×µČŅ©Ąķ×÷ÓĆ£¬ĘäŗĻ³ÉĀ·ĻßČēĻĀ£ŗ

£Ø1£©AµÄĻµĶ³ĆüĆūĪŖ____________£¬EÖŠ¹ŁÄÜĶŵÄĆū³ĘĪŖ____________”£
£Ø2£©A”śBµÄ·“Ó¦ĄąŠĶĪŖ____________£¬“Ó·“Ó¦ĖłµĆŅŗĢ¬ÓŠ»ś»ģŗĻĪļÖŠĢį“æBµÄ³£ÓĆ·½·ØĪŖ____________”£
£Ø3£©C”śDµÄ»Æѧ·½³ĢŹ½ĪŖ________________________”£
£Ø4£©CµÄĶ¬·ÖŅģ¹¹ĢåW£Ø²»æ¼ĀĒŹÖŠŌŅģ¹¹£©æÉ·¢ÉśŅų¾µ·“Ó¦£ŗĒŅ1 mol W×ī¶ąÓė2 mol NaOH·¢Éś·“Ó¦£¬²śĪļÖ®Ņ»æɱ»Ńõ»Æ³É¶žŌŖČ©”£Āś×ćÉĻŹöĢõ¼žµÄWÓŠ____________ÖÖ£¬ČōWµÄŗĖ“Ź²ÕńĒāĘ×¾ßÓŠĖÄ×é·å£¬ŌņĘä½į¹¹¼ņŹ½ĪŖ____________”£
£Ø5£©FÓėGµÄ¹ŲĻµĪŖ£ØĢīŠņŗÅ£©____________”£
a£®Ģ¼Į“Ņģ¹¹ b£®¹ŁÄÜĶÅŅģ¹¹ c£®Ė³·“Ņģ¹¹ d£®Ī»ÖĆŅģ¹¹
£Ø6£©MµÄ½į¹¹¼ņŹ½ĪŖ____________”£
£Ø7£©²ĪÕÕÉĻŹöŗĻ³ÉĀ·Ļߣ¬ŅŌ![]() ĪŖŌĮĻ£¬²ÉÓĆČēĻĀ·½·ØÖʱøŅ½Ņ©ÖŠ¼äĢå
ĪŖŌĮĻ£¬²ÉÓĆČēĻĀ·½·ØÖʱøŅ½Ņ©ÖŠ¼äĢå![]() ”£
ӣ

øĆĀ·ĻßÖŠŹŌ¼ĮÓėĢõ¼ž1ĪŖ____________£¬XµÄ½į¹¹¼ņŹ½ĪŖ____________£»
ŹŌ¼ĮÓėĢõ¼ž2ĪŖ____________£¬YµÄ½į¹¹¼ņŹ½ĪŖ____________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com