
【题目】某有机物F(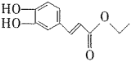 )在自身免疫性疾病的治疗中有着重要的应用,工业上以乙烯和芳香族化合物B为基本原料制备F的路线图如下:
)在自身免疫性疾病的治疗中有着重要的应用,工业上以乙烯和芳香族化合物B为基本原料制备F的路线图如下:
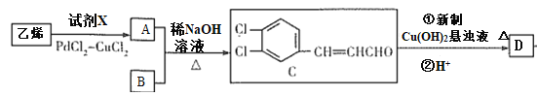
已知:RCHO+CH3CHO![]() RCH=CHCHO
RCH=CHCHO
(1)乙烯生成A的原子利用率为100%,则X是___________(填化学式),F中含氧官能团的名称为___________。
(2)E→F的反应类型为___________,B的结构简式为___________,若E的名称为咖啡酸,则F的名称是___________。
(3)写出D与NaOH溶液反应的化学方程式:_________________________________。
(4)E的同系物G比E多一个碳原子,G有多种同分异构体,符合下列条件的同分异构体有___________种
①能发生水解反应、银镜反应且1mol该物质最多可还原出4 mol Ag
②遇FeCl3溶液发生显色反应
③分子中没有甲基,且苯环上有2个取代基
(5)以乙烯为基本原料,设计合成路线合成2-丁烯酸,写出合成路线:______________________________(其他试剂任选)。
【答案】O2 (酚)羟基、酯基 取代反应(或酯化反应) ![]() 咖啡酸乙酯
咖啡酸乙酯 ![]() +5NaOH
+5NaOH![]() +2NaCl+3H2O 9 CH2=CH2
+2NaCl+3H2O 9 CH2=CH2 ![]() CH3CHO
CH3CHO![]() CH3CH=CHCHO
CH3CH=CHCHO![]() CH3CH=CHCOOH
CH3CH=CHCOOH
【解析】
根据流程图中有机物的结构式、分子式及反应条件分析各步反应的反应类型及产物;根据已知条件分析同分异构体的种类;根据题干信息设计有机物合成路线。由C的结构简式、反应信息知,A、B中均含有醛基,再结合乙烯与A的转化关系知,A是乙醛,B是![]() ,由C转化为D的反应条件知,D为
,由C转化为D的反应条件知,D为![]() ,由E的分子式、F的结构式及反应条件知,E为
,由E的分子式、F的结构式及反应条件知,E为![]() ,由E、F之间的关系知Y是乙醇,由酯的命名方法知F的名称为咖啡酸乙酯;
,由E、F之间的关系知Y是乙醇,由酯的命名方法知F的名称为咖啡酸乙酯;
由C的结构简式、反应信息知,A、B中均含有醛基,再结合乙烯与A的转化关系知,A是乙醛,B是![]() ,由C转化为D的反应条件知,D为
,由C转化为D的反应条件知,D为![]() ,由E的分子式、F的结构式及反应条件知,E为
,由E的分子式、F的结构式及反应条件知,E为![]() ,由E、F之间的关系知Y是乙醇,由酯的命名方法知F的名称为咖啡酸乙酯;
,由E、F之间的关系知Y是乙醇,由酯的命名方法知F的名称为咖啡酸乙酯;
(1)乙烯生成乙醛,则X是O2;F中含氧官能团的名称为羟基、酯基;
(2)E→F的反应类型为酯化反应或取代反应;B的结构简式为![]() ;F的名称是咖啡酸乙酯;
;F的名称是咖啡酸乙酯;
(3)D为![]() ,与NaOH溶液反应的化学方程式:
,与NaOH溶液反应的化学方程式:![]() ;
;
(4)由②得出分子中含有苯环且苯环上含有酚羟基;由①及分子中氧原子数目知分子中含有一个-CHO、一个HCOO-,苯环上有2个官能团一定有-OH,还含有-CH2CH(CHO)OOCH或-CH(CHO)CH2OOCH或-CH(OOCH)CH2CHO,苯环上有3种不同的位置关系,故共有9种同分异构体;
(5)乙烯先被氧化成乙醛,乙醛再转化为2-丁烯醛,最后氧化为目标产物: CH2=CH2 ![]() CH3CHO
CH3CHO![]() CH3CH=CHCHO
CH3CH=CHCHO![]() CH3CH=CHCOOH。
CH3CH=CHCOOH。


科目:高中化学 来源: 题型:
【题目】20℃时,在H2C2O4、NaOH混合溶液中,c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol/L。含碳元素微粒的分布分数δ随溶液pH变化的关系如图所示。下列说法正确的是( )
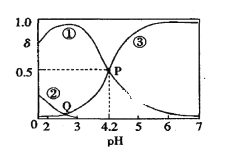
A. ①表示H2C2O4的分布曲线,③表示C2O42-的分布曲线
B. 20℃时,H2C2O4的二级电离平衡常数Ka2=1×10-4.2
C. Q点对应溶液中lgc(H+)<lgc(OH-)
D. 0.100mol·L-1的NaHC2O4溶液中:c(OH-)=c(H+)-2c(C2O42-)+c(H2C2O4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaClO2在水溶液中能发生水解。常温时,有1 mol/L的HClO2溶液和1mol/L的HBF4(氟硼酸)溶液起始时的体积均为V0,分别向两溶液中加水,稀释后溶液的体积为V,所得曲线如图所示。下列说法错误的是
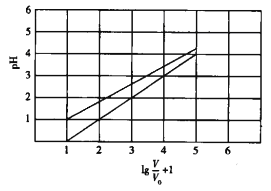
A. HClO2为弱酸,HBF4为强酸
B. 常温下HClO2的电高平衡常数的数量级为10—4
C. 在0≤pH≤5时,HBF4溶液满足pH=lg(V/V0)
D. 25℃时1L pH=2的HBF4溶液与100℃时1L pH=2的HBF4溶液消耗的NaOH相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向20mL 0.1mol/L氨水中通入HCl气体,溶液中由水电离出的氢离子浓度随通入HCl气体的体积变化如图所示。则下列说法正确的是
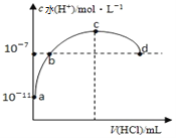
A. b点通入的HCl气体,在标况下为44.8mL
B. b、c之间溶液中c(NH4+)>c(Cl-)
C. 取10mL的c点溶液稀释时:c(NH4+)/c(NH3·H2O)减小
D. d点溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物完全燃烧生成CO2和H2O。将12.4 g该有机物的完全燃烧产物通过浓硫酸,浓硫酸增重10.8 g,再通过碱石灰,碱石灰增重了17.6 g。下列说法不正确的是
A. 该有机物的最简式为CH3O
B. 该有机物的分子式可能为CH3O
C. 该有机物的分子式一定为C2H6O2
D. 该有机物可能属于醇类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标出下列氧化还原反应的电子转移数目和方向,并写出氧化剂
(1)2K2S + K2SO3 + 3H2SO4= 3K2SO4 + 3S↓+ 3H2O _______氧化剂_______
(2)2KMnO4 +5H2O2 + 3H2SO4 = K2SO4+2MnSO4+5O2↑ + 8H2O _______ 氧化剂_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中溴含量约为 65 mg·L-1,从海水中提取溴的工艺流程如下:

(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是____________。
(2)步骤Ⅱ通入热空气吹出Br2,利用了溴的____。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数:_____![]()
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:__________。
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是____。
A.乙醇 B.四氯化碳 C.烧碱溶液 D.苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学向一定体积的Ba(OH)2溶液中逐滴加入稀硫酸,并测得混合液的导电能力随时间变化曲线如图,该小组同学据图分析错误的是

A.AB段溶液的导电能力不断减弱,说明电解质逐渐转变为非电解质
B.B处的导电能力为0,说明溶液中几乎没有自由移动的离子
C.BC段溶液的导电能力不断增大,主要是由于过量的Ba(OH)2电离出的离子导电
D.a时刻Ba(OH)2溶液中与稀硫酸恰好完全中和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,两种碳酸盐![]() ,(
,(![]() 分别为Ca2+和Ba2+两种离子)的沉淀溶解平衡曲线如图所示。已知:
分别为Ca2+和Ba2+两种离子)的沉淀溶解平衡曲线如图所示。已知:![]() ,
,![]() 。已知
。已知![]() 比
比![]() 溶解度更大(不考虑阴离子的水解)。下列说法正确的是
溶解度更大(不考虑阴离子的水解)。下列说法正确的是
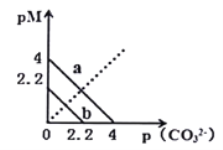
A. 向![]()
![]() 的
的![]() 溶液中加入固体
溶液中加入固体![]() ,当加入
,当加入![]() 固体的质量为
固体的质量为![]() 时,
时,![]() 恰好沉淀完全(离子浓度为
恰好沉淀完全(离子浓度为![]() 时认为沉淀完全;忽略溶液体积变化)
时认为沉淀完全;忽略溶液体积变化)
B. ![]() 的
的![]()
C. 该温度下,向![]() 的饱和溶液中加入
的饱和溶液中加入![]() 溶液,一定能产生沉淀
溶液,一定能产生沉淀
D. 线![]() 表示
表示![]() 的溶解平衡曲线
的溶解平衡曲线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com