
| 实验 | 反应温度/℃ | Na2S2O3溶液 | 稀H2S4 | H2O | ||
| V/mL | c(mol?L-1) | V/mL | c(mol?L-1) | V/mL | ||
| A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
| C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
| D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
| A、A | B、B | C、C | D、D |
科目:高中化学 来源: 题型:
| A、胶体是一种带电的分散系 |
| B、可以用丁达尔现象区别胶体与溶液 |
| C、胶体和浊液不能透过滤纸而溶液可以 |
| D、向氢氧化铁胶体中加入硫酸钠不能出现沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜锌原电池工作时,电子从负极出发沿外电路回到正极 |
| B、原电池的负极发生还原反应 |
| C、甲醇燃料电池可把化学能转化为电能 |
| D、锌锰干电池中,锌电极是负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaO+H2O=Ca(OH)2 |
| B、2Na+2H2O=2NaOH+H2↑ |
| C、2F2+2H2O=4HF+O2 |
| D、HCl+NaOH=NaCl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Ba2、NO3-、HCO3- |
| B、Cl-、K+、H+、Na+、SO42- |
| C、MnO4-、K+、Cl-、Mn2+ |
| D、Fe2+、NO3-、SO42-、OH-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
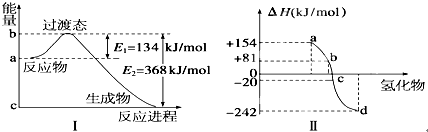
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com