
| A. | 粗盐可采用除杂和重结晶等过程提纯 | |
| B. | 工业生产中常选用石灰乳作为 Mg2+的沉淀剂 | |
| C. | 第②步的反应条件是:在空气中直接加热 | |
| D. | 第③步到第⑤步的目的是为了富集溴元素 |
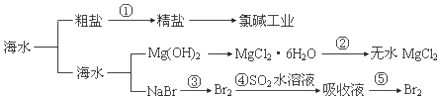
分析 海水蒸发溶剂得到粗盐和母液,粗盐通过精制得到精盐,电解饱和食盐水得到氯气、氢气和氢氧化钠;母液加氢氧化钠反应生成氢氧化镁沉淀,氢氧化镁和酸反应生成氯化镁,制得氯化镁,母液通入氯气氧化溴离子为溴单质,被二氧化硫吸收后发生氧化还原反应生成溴化氢,富集溴元素,通入氯气氧化溴化氢为溴单质得到高浓度的溴,以此解答该题.
解答 解:A.粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时通常在溶液中依次中加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性,再进行重结晶进行提纯,故A正确;
B.工业生成处于生石灰或石灰水作沉淀剂,生成氢氧化镁沉淀,故B正确;
C.氯化镁晶体失去结晶水关键是需要防止其水解,应在氯化氢气流中加热失去结晶水,故C错误;
D.第③步将溴离子被氧化为溴单质,第④步中溴单质被还原为溴离子,第⑤步中溴离子被氧化为溴单质,过程的目的是浓缩富集溴元素,故D正确.
故选C.
点评 本题考查海水资源综合应用,为高频考点,把握流程中的转化、混合物分离提纯及电解等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:解答题
| 离子 | 开始沉淀pH | 沉淀完全pH |
| Fe2+ | 7.6 | 9.6 |
| Fe3+ | 2.7 | 3.7 |
| Zn2+ | 5.4 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁溶于氢碘酸溶液中:Fe(OH)3+3HI═Fe3++3I-+3H2O | |
| B. | 少量CO2通入苯酚钠溶液中: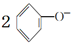 +H2O+CO2→ +H2O+CO2→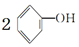 +CO32- +CO32- | |
| C. | 向NaAlO2溶液中通入足量CO2:2AlO2-+3H2O+CO2═2Al(OH)3↓+CO32- | |
| D. | Ca(HCO3)2溶液与足量NaOH溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2(HCl):通过水洗涤 | B. | NO(NH3):通过水洗涤 | ||
| C. | NH4Cl(I2):加热混合物 | D. | NH4Cl溶液(I2):用CCl4萃取 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 3:1 | C. | 3:2 | D. | 2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
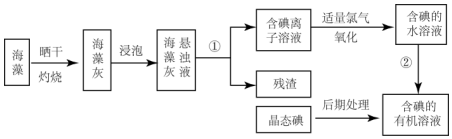
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 8种 | C. | 32种 | D. | 64种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C7H16主链上有5个碳原子的同分异构体有5种 | |
| B. | 按系统命名法,化合物的名称是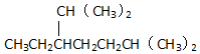 2,6-二甲基-3-乙基庚烷 2,6-二甲基-3-乙基庚烷 | |
| C. | 乙炔分子的球棍模型: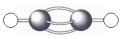 | |
| D. | 卤代烃加入硝酸酸化的硝酸银溶液根据生成的卤化银沉淀颜色检验卤原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com