
| A. | 氨气分子的电子式: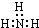 | B. | S2-的结构示意图: | ||
| C. | CH4的球棍模型示意图为: | D. | 用电子式表示HCl形成过程: |
分析 A.氨气分子的电子式中漏掉了氮原子的1对未成键电子;
B.阴离子的核外电子数大于核内质子数;
C.根据甲烷的球棍模型与比例模型进行判断;
D.
解答 解:A.氨气分子中氮原子最外层达到8电子稳定结构,漏掉了氮原子的一对孤电子对,氨气的电子式为 ,故A错误;
,故A错误;
B.S2-的离子结构示意图为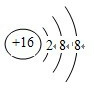 ,故B正确;
,故B正确;
C. 为甲烷的比例模型,甲烷的球棍模型应该用小球和短棍表示,甲烷为正四面体结构,其正确的球棍模型为:
为甲烷的比例模型,甲烷的球棍模型应该用小球和短棍表示,甲烷为正四面体结构,其正确的球棍模型为: ,故C错误;
,故C错误;
D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、元素符号、离子结构示意图、电子排布式等知识,明确常见化学用语的书写原则为解答结构,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:选择题
| A. | 能使酸性KMnO4溶液褪色,说明SO2具有漂白性 | |
| B. | 能使澄清石灰水变浑浊 | |
| C. | 不能与NaOH溶液反应 | |
| D. | 能与水反应生成硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5min内P的平均反应速率为0.15mol/(L•min) | |
| B. | Q的平衡浓度为1mol/L | |
| C. | Q的转化率为25% | |
| D. | x是2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解过程中阴极没有气体生成 | |
| B. | 电解过程中转移的电子的物质的量为0.4 mol | |
| C. | 原CuSO4溶液的浓度为0.1 mol•L-1 | |
| D. | 电解过程中阳极收集到的气体体积为2.24 L(标况下) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;A、B、D的熔点依次增大的顺序为SiO2>NaF>P4.
;A、B、D的熔点依次增大的顺序为SiO2>NaF>P4.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 混合物 | 分离方法 | 操作过程 | |
| 1 | 从草木灰中提取可溶性物质 | 溶解、过滤 | 将草木灰溶于热水中,不断搅拌, 然后过滤.若滤液仍浑浊,再过滤 |
| 2 | KNO3和NaCl混合物 | 结晶、过滤 | 将混合物溶于热水配成饱和溶液降温,溶液中有KNO3晶体析出,冷却过滤 |
| 3 | 由乙醇溶液制无水乙醇 | 蒸馏 | 加入一定量的生石灰,然后蒸馏 |
| 4 | 除去淀粉溶液中的碘化钠 | 渗析 | 将混合液放入半透膜袋中,并放入流动的蒸馏水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
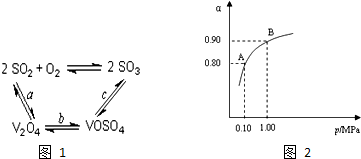 工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收.请回答下列问题:
工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收.请回答下列问题: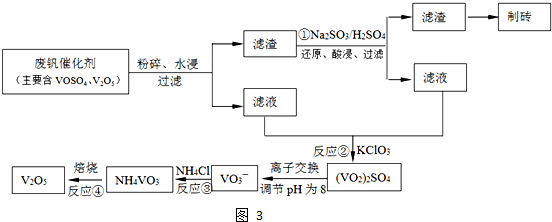
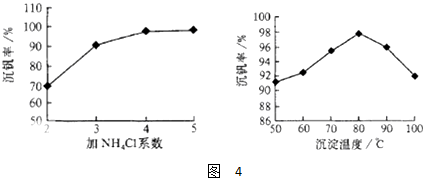
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b>c>d | B. | a>c>d>b | C. | c>a>b>d | D. | b>d>c>a |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com