
【题目】下列过程没有发生化学反应的是( )
A、用活性炭去除冰箱中的异味
B、用热碱水清除炊具上残留的油污
C、用浸泡过高锰酸钾溶液的硅藻土保存水果
D、用含硅胶、铁粉的透气小袋与食品一起密封包装
科目:高中化学 来源: 题型:
【题目】某校研究性学习小组的同学设计了如图所示的实验装置(夹持及尾气处理装置未画出)来探究氨气的性质。A中是氯化铵和氢氧化钙固体,C中盛Wg固体氧化铜。实验时观察到C中CuO变为红色,D中无水CuSO4变蓝,同时生成一种无污染的气体。

回答下列问题:
(1)B中碱石灰的作用是____________。
(2)氨气与CuO反应的化学方程式为 。该反应中氨的作用是______(填氧化剂或还原剂)。
(3)有同学认为NH3与CuO反应生成的红色物质中可能含Cu2O。Cu2O在酸性溶液中Cu+歧化生成Cu和Cu2+。请设计一个简单的实验检验该红色物质中是否含有Cu2O 。
(4)若实验前后D装置的质量差为ag,则制得的铜的纯度为____________(用含a和 W的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B、C和气体乙、丙及物质D、E、F、G、H,它们之间发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
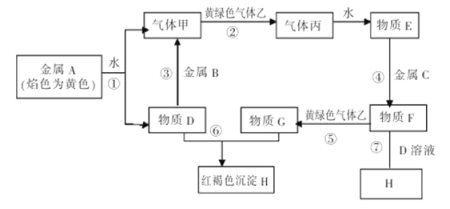
请根据以上信息回答下列问题:
(1)物质F的化学式为 。
(2)说出黄绿色气体乙的一种用途 。
(3)区别E、F两种溶液最简单的方法是 ,实验室检验G中所含的金属离子时,常在G的溶液中加入 溶液。
(4)反应①的离子方程式为 。
(5)物质F→H的转化需经过两个连续进行的反应,请写出这两个反应的化学方程式: 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有下列六种离子:①HCO3﹣②SO32﹣③Na+④CO32﹣⑤NH4+⑥NO3﹣,向其中加入一定量Na2O2后,溶液中离子浓度基本保持不变的是( )
A. 只有⑥ B. ④⑥ C. ③④⑥ D. ①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化铈(CeO2)是一种重要的稀土氧化物。以氟碳铈矿(主要含CeFCO3)为原料制备CeO2的一种工艺流程如下:
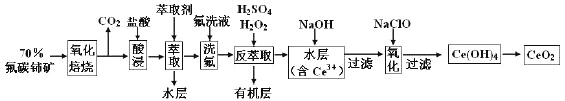
已知:①Ce4+既能与F-结合成[CeFx](4-x)+,也能与SO42-结合成[CeSO4]2+;
②在硫酸体系中Ce4+能被萃取剂[(HA)2]萃取,而Ce3+不能。
回答下列问题:
(1)“氧化焙烧”前需将矿石粉碎成细颗粒,其目的是__________________________。
(2)“酸浸”中会产生大量黄绿色气体,写出CeO2与盐酸反应的离子方程式:_________________________________;为避免产生上述污染,请提出一种解决方案:________。
(3)“萃取”时存在反应:Ce4++n(HA)2 ![]() Ce·(H2n-4A2n)+4H+。实验室中萃取时用到的主要玻璃仪器名称为___________; ____________________________________________________________。
Ce·(H2n-4A2n)+4H+。实验室中萃取时用到的主要玻璃仪器名称为___________; ____________________________________________________________。
(4)“反萃取”中,在稀硫酸和H2O2的作用下CeO2转化为Ce3+,H2O2在该反应中作_________(填“催化剂”、“氧化剂”或“还原剂”),每有1mol H2O2参加反应,转移电子的物质的量为________________。
(5)“氧化”步骤的化学方程式为________________________________。
(6)取上述流程中得到的CeO2产品0.4500g,加硫酸溶解后,用0.1000mol/LFeSO4标准溶液滴定至终点时(铈被还原为Ce3+,其它杂质均不反应),消耗25.00mL标准溶液。该产品中CeO2的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,既能因发生化学反应使溴水褪色,又能使酸性KMnO4溶液褪色的是
①SO2 ②CH3CH2CH=CH2③![]() ④CH3CH3
④CH3CH3
A. ①②③④ B. ③④ C. ①②④ D. ①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:
C(金刚石,s)+O2(g)===CO2(g) ΔH1
C(石墨,s)+O2(g)===CO2(g) ΔH2
C(石墨,s)===C(金刚石,s) ΔH3=+1.9 kJ·mol-1
下列说法正确的是( )
A.石墨转化成金刚石的反应是吸热反应
B.金刚石比石墨稳定
C.ΔH3=ΔH1-ΔH2
D.ΔH1>ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出257.7kJ的热量(相当于25℃、101 kPa下测得的热量)。反应的热化学方程式为 。又已知H2O(l)=H2O(g) ΔH=+44kJ/mol。则16g液态肼与过氧化氢反应生成液态水时放出的热量是 kJ。
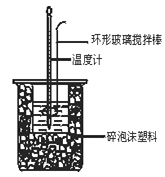
(2)分别取40 mL 0.50 mol/L盐酸与 0.55 mol/L NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
假设盐酸和氢氧化钠溶液的密度都是1 g/cm3,又知中和后生成溶液的比热容c = 4.18 J/(g·℃)。实验时,还需测量的数据有 。
A.反应前盐酸溶液的温度
B.反应前盐酸溶液的质量
C.反应前氢氧化钠溶液的温度
D.反应前氢氧化钠溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
某学生实验记录数据如下:
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | 氢氧化钠 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热为ΔH = ____________。
假定该学生的操作完全同上,实验中改用100 mL 0.50 mol/L盐酸跟100 mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com