
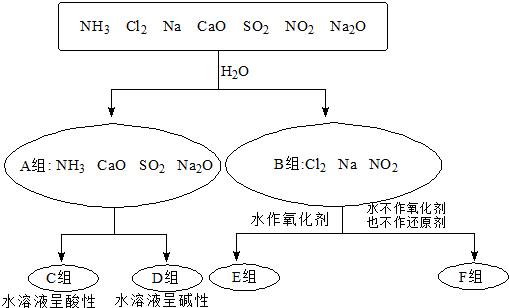
分析 (1)A组中物质与水发生反应,元素的化合价没有发生变化,而B组中物质与水发生氧化还原反应,依据图表变化和物质分类分析变化判断;
(2)F组与水反应时,水既不是氧化剂又不是还原剂,结合三种物质与水反应的特点判断.
(3)水作氧化剂的反应是金属钠和水之间的反应;
(4)氯气具有氧化性,二氧化硫具有还原性,二者在水溶液中可以发生氧化还原反应;
(5)一水合氨电离出氢氧根离子而使其溶液呈碱性;
(6)氢氧化铝是两性氢氧化物溶于强酸强碱.
解答 解:(1)A组中物质与水发生反应,元素的化合价没有发生变化,不是氧化还原反应,而B组中物质与水发生氧化还原反应,则A、B的分组从是否发生氧化还原反应的角度分类,故答案为:是否发生氧化还原反应;
(2)F组与水反应时,水既不是氧化剂又不是还原剂,应为氯气、二氧化氮与水的反应,与水反应时发生反应的方程式为3NO2+H2O═2HNO3+NO即3NO2+H2O═2H++2NO3-+NO,反应二氧化氮中氮元素化合价既升高也降低,二氧化氮既作氧化剂又作还原剂,故答案为:NO2;3NO2+H2O═2H++2NO3-+NO;
(3)水作氧化剂的反应是金属钠和水之间的反应,即2Na+2H2O═2NaOH+H2↑;故答案为:2Na+2H2O═2NaOH+H2↑;
(4)氯气具有氧化性,二氧化硫具有还原性,二者在水溶液中可以发生氧化还原反应SO2+Cl2+2H20═H2SO4+2HCl,故答案为:SO2+Cl2+2H20═H2SO4+2HCl;
(5)氨水呈弱碱性是因为一水合氨存在电离平衡电离出氢氧根离子,电离方程式为:NH3•H2O?NH4++OH-,故答案为:NH3•H2O?NH4++OH-;
(6)氢氧化铝是两性氢氧化物溶于强酸强碱,过量NaOH会溶解生成的沉淀,离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O.
点评 本题考查物质的分类和二氧化硫的化学性质以及热化学方程式的书写以及盖斯定律的应用知识,注意知识之间的联系,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 分子里含有碳碳三键的脂肪烃 | |
| B. | 易发生加成反应 | |
| C. | 既能使溴水褪色也能使酸性高锰酸钾溶液褪色 | |
| D. | 分子里所有的碳原子都处在同一条直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(s)+O2(g)=CO2(g)△H=+110.5 kJ/mol | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.31 kJ/mol | |
| C. | H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8 kJ/mol | |
| D. | 2C8H18(l)+25O2(g)=16CO2(g)+18H2O(l)△H=-11036 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的燃烧热为890.3 kJ•mol-1,则甲烷燃烧热的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)$?_{30MP}^{500℃}$ 2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 已知在120℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242 kJ•mol-1 | |
| D. | 25℃、101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ•mol-1,硫酸溶液与氢氧化钾溶液反应的热化学方程式为H2SO4(aq)+2KOH(aq)═K2SO4(aq)+2H2O(l)△H=-57.3 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
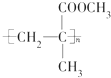 .下列关于它的叙述中不正确的是( )
.下列关于它的叙述中不正确的是( )| A. | 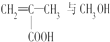 在一定条件下发生缩聚反应即可合成该有机玻璃 在一定条件下发生缩聚反应即可合成该有机玻璃 | |
| B. | 该有机玻璃能发生氧化反应 | |
| C. | 合成该有机玻璃的原料可能有甲烷 | |
| D. | 它在一定条件下发生水解反应时C-O键断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
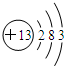 .
.| 元素 | Na | Mg | Al | Si | P | S | Cl |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com