
| A. | 生理盐水指质量分数为0.9%的NaCl溶液 | |
| B. | 1L 0.2mol/L硫酸铁溶液中含有的SO42-的离子数为0.2NA | |
| C. | 1L 1 mol/L K2CO3溶液中含有的钾离子数目为NA | |
| D. | 0.1 mol/L BaCl2溶液中,Cl-的物质的量浓度为0.1 mol/L |
分析 A.医院常用的生理盐水是溶质的质量分数为0.9%的氯化钠溶液;
B.根据n=cV计算出硫酸铁的物质的量,硫酸铁的化学式中含有3个硫酸根离子;
C.碳酸钾的化学式中含有2个钾离子,根据n=cV计算出碳酸钾的物质的量,然后计算出钾离子的物质的量;
D.氯离子浓度为氯化钡浓度的2倍.
解答 解:A.生理盐水的溶质为NaCl,在质量分数为0.9%时能维持细胞的生理形态,则生理盐水是质量分数为0.9%的氯化钠溶液,故A正确;
B.1L 0.2mol/L硫酸铁溶液中含有0.2mol硫酸铁,含有0.6mol硫酸根离子,则含有的SO42-的离子数为0.6NA,故B错误;
C.1L 1 mol/L K2CO3溶液中含有1mol碳酸钾,含有2mol钾离子,含有的钾离子数目为2NA,故C错误;
D.0.1 mol/L BaCl2溶液中,Cl-的物质的量浓度为:0.1mol/L×2=0.2mol/L,故D错误;
故选A.
点评 本题考查了物质的量的简单计算,题目难度不大,明确物质的量与物质的量浓度、阿伏伽德罗常数之间的关系即可解答,试题侧重基础知识的考查,培养了学生的化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 合金完全溶解后产生的H2的物质的量为0.24mol | |
| B. | 合金中的镁与铝的物质的量之比小于1 | |
| C. | 若向溶液X中加入270mL2.0mol•L-1NaOH溶液,充分反应,所得沉淀为Mg(OH)2 | |
| D. | 若向溶液X中加入足量的氨水,充分反应,所得沉淀经过过滤、洗涤后充分灼烧,则残留固体质量大于8.50g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向淀粉溶液中加入稀硫酸加热后,再用NaOH中和,并做银镜反应实验--检验淀粉是否水解 | |
| B. | 向甲酸和甲醛的混合物中加入氢氧化钠溶液,中和甲酸后,加入新制的氢氧化铜加热:检验混合物中是否含有甲醛 | |
| C. | 向米汤中加入含碘的食盐,观察是否有颜色的变化--检验含碘食盐中是否含碘酸钾 | |
| D. | 检验某溴乙烷中的溴元素可向其中加入AgNO3溶液,观察有无浅黄色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 粗盐先通过除杂、精制得到饱和食盐水,然后电解得到氯气,最后和石灰乳反应制得漂白粉 | |
| B. | 苦卤酸化后通入氯气得到溴水,然后用热空气将其通入到SO2水溶液中,最后通入氯气后蒸馏得粗溴 | |
| C. | 干海带灼烧后加水浸取,然后加入H2O2得到碘水,最后通过萃取、分液、蒸馏得到碘单质 | |
| D. | 向海水中加入石灰乳得到Mg(OH)2,加入盐酸得到MgCl2溶液,最后电解该溶液得到镁单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
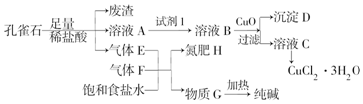
| 金属离子 | Fe3+ | Fe2+ | Cu2+ | |
| pH | 氢氧化物开始沉淀 | 1.9 | 7.0 | 4.7 |
| 氢氧化物安全沉淀 | 3.2 | 9.0 | 6.7 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
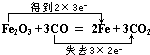
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com