
【题目】实验室制乙烯,常因温度过高生成少量SO2,有人设计了如图所示实验,以验证上述混合气体中是否含有乙烯和SO2。

(1)在烧瓶中除了加入乙醇、浓硫酸外,还应放入几块碎瓷片,其目的是:____。
(2)写出生成乙烯的反应方程式:____。
(3)Ⅱ、Ⅲ、Ⅳ、Ⅴ、装置中盛放的试剂是(从下列所给试剂中选出,填序号)
①品红溶液,②NaOH溶液,③酸性KMnO4溶液。则正确的排列顺序为:_____。
(4)能说明SO2气体存在的现象是____。
(5)确证含有乙烯的现象是____。
【答案】防止暴沸 C2H5OH![]() CH2=CH2↑ +H2O ①②①③ Ⅱ中品红溶液褪色 Ⅳ中品红溶液不褪色,Ⅴ中酸性KMnO4溶液褪色
CH2=CH2↑ +H2O ①②①③ Ⅱ中品红溶液褪色 Ⅳ中品红溶液不褪色,Ⅴ中酸性KMnO4溶液褪色
【解析】
由实验装置图可知,装置Ⅰ中乙醇在浓硫酸作用下,加热到170℃发生消去反应生成乙烯和水,实验是需要用温度计控制反应温度,需要加入碎瓷片防止暴沸;装置Ⅱ中盛有品红溶液,用于检验二氧化硫的生成;装置Ⅲ中盛有氢氧化钠溶液,用于吸收二氧化硫,防止二氧化硫干扰乙烯的检验;装置Ⅳ盛有品红溶液,用于证明二氧化硫被完全吸收;装置Ⅴ盛有酸性KMnO4溶液,用于检验乙烯的生成。
(1)液体加热时会发生暴沸现象,为防止暴沸发生,常加入几块碎瓷片,故答案为:防止暴沸;
(2)乙醇在浓硫酸作用下,加热到170℃发生消去反应生成乙烯和水,反应的化学方程式为C2H5OH![]() CH2=CH2↑ +H2O,故答案为:C2H5OH
CH2=CH2↑ +H2O,故答案为:C2H5OH![]() CH2=CH2↑ +H2O;
CH2=CH2↑ +H2O;
(3)乙烯和SO2都具有还原性,都能使酸性KMnO4溶液褪色,为防止二氧化硫干扰乙烯的检验,应先检验并吸收二氧化硫,则装置Ⅱ中盛有品红溶液,用于检验二氧化硫的生成;装置Ⅲ中盛有氢氧化钠溶液,用于吸收二氧化硫,防止二氧化硫干扰乙烯的检验;装置Ⅳ盛有品红溶液,用于证明二氧化硫被完全吸收;装置Ⅴ盛有酸性KMnO4溶液,用于检验乙烯的生成,故答案为:①②①③;
(3)装置Ⅱ中盛有品红溶液,用于检验二氧化硫的生成,装置Ⅱ中的品红溶液褪色说明存在二氧化硫气体,故答案为:Ⅱ中品红溶液褪色;
(4)装置Ⅳ中的品红不褪色,说明二氧化硫已除尽,装置Ⅴ中的高锰酸钾褪色,说明存在乙烯气体,故答案为:Ⅳ中品红溶液不褪色,Ⅴ中酸性KMnO4溶液褪色。


科目:高中化学 来源: 题型:
【题目】CuO有氧化性,能被NH3还原,为验证此结论,设计如下实验。
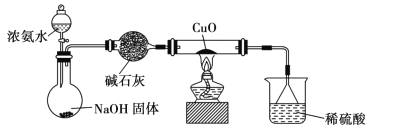
有关该实验的说法正确的是
A.反应时生成一种无污染的气体NO
B.NH3与CuO反应后生成的红色物质可能是Cu
C.装浓氨水的装置名称是分液漏斗,只能用作分液操作
D.烧杯中硫酸的作用是防倒吸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作或实验现象的解释(方程式)正确的是
A.除去Na2CO3溶液中的Na2SO4,加入适量Ba(OH)2溶液后,过滤:Ba2++![]() =BaSO4↓
=BaSO4↓
B.向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2=Ag2S↓+2Cl
C.Na2O2在潮湿的空气中放置一段时间,变成白色黏稠物:2Na2O2+2CO2=2Na2CO3+O2
D.向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀: 2![]() +Ca2++2OH=CaCO3↓+
+Ca2++2OH=CaCO3↓+![]() +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列原子或原子团,请按要求选择两个,写出符合要求的有机物的结构简式:﹣CH3、﹣OH、﹣CHO、﹣COOH、﹣Br、﹣H、﹣CH2CH3、![]()
(l)分子结构为正四面体的是:___;
(2)能使FeCl3溶液显紫色的是:___;
(3)在NaOH乙醇溶液中能发生消去反应的是:____;
(4)1mol该有机物与足量的银氨溶液反应,有4molAg生成的是:___;
(5)相对分子质量是60,能和NaHCO3反应放出CO2的是:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知几种物质之间的能量关系如图所示, 下列说法中正确的是
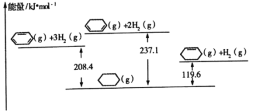
A.使用合适催化剂,能减小反应的焓变
B.![]() +H2(g)
+H2(g)![]()
![]() (g) ΔH=+28.7kJ/mol
(g) ΔH=+28.7kJ/mol
C.![]() (g)中,热能转化为产物内部的能量
(g)中,热能转化为产物内部的能量
D.![]() (g),反应物的总能量低于生成物的总能量
(g),反应物的总能量低于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁铝合金5.1 g溶于300 mL2 mol·L-1盐酸中,标准状况下放出气体的体积为5.6 L,向反应后的溶液中加入500 mLNaOH溶液充分反应,最终产生白色沉淀。下列有关说法不正确的是
A.5.1 g镁铝合金中含有镁、铝的质量分别为2.4 g、2.7 g
B.溶解5.1 g镁铝合金时,剩余盐酸中溶质的物质的量为0.1 mol
C.若白色沉淀只有Mg(OH)2,该NaOH溶液的物质的量浓度至少为1.2 mol·L-1
D.生成白色沉淀的最大质量为13.6 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铝土矿(主要成分为Al2O3,还含少量Fe2O3、SiO2等)为主要原料生产金属铝的工艺流程如图:下列说法错误的是
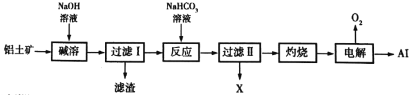
A.碱溶过程发生复杂的氧化还原反应
B.过滤1的滤渣中含Fe2O3、SiO2等
C.X主要溶质是Na2CO3
D.产生Al和O2的电解过程通常使用助熔剂Na3AlF6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃 A 与 Br2 发生加成反应生成二溴代物 B。B 用热的 NaOH 醇溶液处理得有机物 C,经测定 C 的分子中含有 两个双键,其分子式为 C5H6。将 C 在催化条件下加氢可得到分子式为 C5H10 的有机物 D,D 的一氯代物只有 1 种结 构。则烃 A 的结构简式为( )
A.![]() B.CH2=CH—CH2—CH=CH2
B.CH2=CH—CH2—CH=CH2
C.CH3CH2CH2CH=CH2D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:
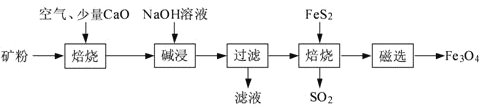
(1)粉碎高硫铝土矿石的目的是___。
(2)第一次焙烧时发生氧化还原反应:___。
(3)碱浸时发生反应的化学方程式为___。
(4)过滤后向滤液中通入过量的CO2气体,反应的离子方程式为___;___。
(5)“过滤”得到的滤渣中含有大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2):n(Fe2O3)=___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com