
【题目】如图为原电池装置示意图。
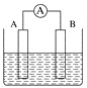
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是_____(填字母)。
A.铝片、铜片 B.铜片、铝片
C.铝片、铝片 D.铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式____
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4===2PbSO4+2H2O。写出B电极反应式___,该电池在工作时,A电极的质量将___(填“增加”“减小”或“不变”)。若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为___。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出A电极反应式:_____;该电池在工作一段时间后,溶液的碱性将_____(填“增强”“减弱”或“不变”)。
【答案】B Al-3e-+4OH-===![]() +2H2O PbO2+
+2H2O PbO2+![]() +4H++2e-===PbSO4+2H2O 增加 0.1NA H2+2OH--2e-===2H2O 减弱
+4H++2e-===PbSO4+2H2O 增加 0.1NA H2+2OH--2e-===2H2O 减弱
【解析】
(1)铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,根据负极金属单质上电子来判断;碱性条件下,Al失电子生成偏铝酸根离子;
(2)B为PbO2,是原电池的正极,发生还原反应,注意电解质溶液是硫酸;A是Pb,其离子能够与硫酸根反应生成沉淀;据电池反应式计算;
(3)氢氧燃料电池中,氢气在负极发生氧化反应,碱性环境中生成水,氢氧燃料电池反应生成水,导致电解质溶液浓度降低。
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,铝钝化,所以Cu失电子作负极,一组插入烧碱溶液中,Cu与氢氧化钠不反应,Al失电子作负极,碱性条件下,Al失电子生成偏铝酸根离子,其电极反应为:Al+4OH--3e-=AlO2-+2H2O;
(2)B为PbO2,是原电池的正极,发生还原反应,电解质溶液是硫酸,铅离子能够与硫酸根离子生成沉淀,电极反应式为:PbO2+SO42-+4H++2e-=PbSO4+2H2O;A极Pb失电子生成铅离子能够与硫酸根反应生成沉淀,导致质量增大;据电池反应式可知,每有2mol硫酸反应转移电子2mol,则0.1mol硫酸反应转移电子数目为0.1NA;
(3)氢氧燃料电池中,氢气在负极发生氧化反应,碱性环境中生成水,A为负极,负极的电极反应式为:H2+2OH--2e-=2H2O,因为生成水,导致电解质溶液的浓度减小,所以KOH溶液的碱性减弱。


科目:高中化学 来源: 题型:
【题目】油脂是油与脂肪的总称,它是多种高级脂肪酸的甘油酯。油脂既是重要食物,又是重要的化工原料。油脂的以下用途与其含有的碳碳不饱和键(![]() )有关的是
)有关的是
A. 衣服上的油脂可用汽油洗去
B. 适量摄入油脂,有利于人体吸收多种脂溶性维生素和胡萝卜素
C. 植物油通过氢化可以制造植物奶油(人造奶油)
D. 脂肪是有机体组织里储存能量的重要物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+立即被还原成Fe2+。据此某学习小组设计如图所示的原电池装置。下列有关说法正确的是
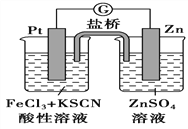
A. 正极反应为Zn-2e-=Zn2+
B. 该电池总反应为3Zn+2Fe3+=2Fe+3Zn2+
C. Pt电极上有气泡出现
D. 左烧杯中溶液的红色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应N2+3H2 ![]() 2NH3的能量变化下图所示,该反应的热化学方程式是
2NH3的能量变化下图所示,该反应的热化学方程式是
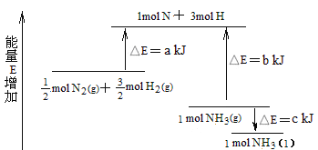
A.N2(g)+3H2(g) ![]() 2NH3(l) △H = 2(a-b+c) kJ/mol
2NH3(l) △H = 2(a-b+c) kJ/mol
B.N2(g)+3H2(g) ![]() 2NH3(l) △H = 2(a-b-c) kJ/mol
2NH3(l) △H = 2(a-b-c) kJ/mol
C.![]() N2(g)+
N2(g)+![]() H2(g)
H2(g) ![]() NH3(l) △H = (b+c-a) kJ/mol
NH3(l) △H = (b+c-a) kJ/mol
D.![]() N2(g)+
N2(g)+![]() H2(g)
H2(g) ![]() NH3(g) △H = (a+b) kJ/mol
NH3(g) △H = (a+b) kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】法国格勒诺布尔(Grenoble)约瑟夫·傅立叶大学的研究小组发明了第一块可植入人体为人造器官提供电能的葡萄糖生物燃料电池,其基本原理是葡萄糖和氧气在人体中酶的作用下发生反应:C6H12O6+6O2![]() 6CO2+6H2O(酸性环境)。下列有关该电池的说法不正确的是( )
6CO2+6H2O(酸性环境)。下列有关该电池的说法不正确的是( )
A. 该生物燃料电池不可以在高温下工作
B. 电池的负极反应为C6H12O6+6H2O-24e-=6CO2↑+24H+
C. 消耗1 mol氧气时转移4 mol e-,H+向负极移动
D. 今后的研究方向是设法提高葡萄糖生物燃料电池的效率,从而使其在将来可以为任何可植入医疗设备提供电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z为短周期元素,X原子的质子数等于Z与Y的质子数之和;Z与Y位于同一周期,Y元素形成气态氢化物水溶液呈碱性,非金属Z的一种固体单质可导电。回答下列问题:
(1)Y在周期表中的位置是第_____周期、第____族,其原子结构示意图为_______.Y与Z之间形成的化学键属于___________(填离子键或共价键)。
(2) X、Y、Z三种元素中原子半径最大的是_______(填元素符号);X单质既可与盐酸反应,又可溶于氢氧化钠溶液,产生的气体为________(填分子式),该气体与Y单质反应的化学方程式______。
(3)Z的最价氧化物的电子式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性溶液中,能大量共存的离子是( )
A.Mg2+、Fe2+、NO3—、Cl—B.Al3+、Fe2+、Cl—、SO42—
C.K+、Na+、Cl—、HCO3— D.Na+、Ba2+、NO3—、SO42—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能存在Fe3+、Fe2+、I-、HCO![]() 、Cl-、NO
、Cl-、NO![]() 六种离子中的几种。进行下列实验:
六种离子中的几种。进行下列实验:
①取少量溶液滴加KSCN溶液,溶液呈红色;
②另取少量原溶液滴加盐酸,溶液的棕黄色加深。
据此可以推断,该溶液中一定大量存在的阴离子是( )
A. I- B. HCO![]() C. Cl- D. NO
C. Cl- D. NO![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com