
【题目】某溶液可能含OH-、SO42-、HCO3-、Cl-、Ba2+和Na+。探究小组为了确定该溶液中离子的组成,取该溶液100mL进行以下实验:
(1)填写下表空格
实验操作与现象 | 实验结论 | 判断理由 | |
步骤一 | 加入过量HCl溶液,有气泡产生; | 肯定有___、肯定无___。 | HCO3-与OH-不共存 |
步骤二 | 步骤一中得到标况下的气体22.4L; | HCO3-的物质的量浓度为___mol/L | C元素守恒 |
步骤三 | 向上述滤液中加足量Ba(NO3)2溶液,经过滤得到46.6g不溶于稀硝酸的沉淀。 | 肯定有___、___;肯定无___。 | 溶液显电中性;SO42-与Ba2+不共存会产生白色沉淀。 |
(2)步骤三过滤所需玻璃仪器有:烧杯、___、___。
(3)步骤一产生气泡的离子方程式为___,步骤三生成沉淀的离子方程式为:___。
【答案】HCO3- OH- 10 SO42- Na+ Ba2+ 漏斗 玻璃棒 HCO3-+H+=CO2↑+H2O Ba2++SO42-=BaSO4↓
【解析】
步骤一:加入过量的HCl产生气泡,说明有HCO3-,则没有OH-;步骤二:HCl和HCO3-反应生成CO2 22.4L(标况),根据元素守恒可以推出原溶液中有1mol HCO3-,从而计算出HCO3-的物质的量浓度;根据步骤三可以推出原溶液中有SO42-,则溶液中无Ba2+,有Na+。
(1)步骤一:加入过量的HCl产生气泡,说明有HCO3-,则没有OH-,因为HCO3-与OH-不共存;步骤二:HCl和HCO3-反应生成CO2 22.4L(标况),n(CO2)=![]() =1mol,则n(HCO3-)=1mol,故c(HCO3-)=
=1mol,则n(HCO3-)=1mol,故c(HCO3-)=![]() =10mol/L;步骤三:根据题中信息,可以推出该沉淀为BaSO4,则n(BaSO4)=
=10mol/L;步骤三:根据题中信息,可以推出该沉淀为BaSO4,则n(BaSO4)=![]() =0.2mol,故原溶液中有0.2mol SO42-,则溶液中无Ba2+,有Na+;
=0.2mol,故原溶液中有0.2mol SO42-,则溶液中无Ba2+,有Na+;
(2)过滤所需玻璃仪器有:烧杯、漏斗、玻璃棒;
(3)步骤一产生气泡的离子方程式为HCO3-+H+=CO2↑+H2O;步骤三生成沉淀的离子方程式为:Ba2++SO42-=BaSO4↓。


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】类推思维是化学解题中常用的一种思维方法,下列有关反应方程式(或离子方程式)的类推正确的是( )
已知 | 类推 | |
A | 将Fe加入CuSO4溶液中: Fe + Cu2+ = Cu + Fe2+ | 将Na加入到CuSO4溶液中: 2Na + Cu2+ = Cu + 2Na+ |
B | 稀硫酸与Ba(OH)2溶液反应至溶液呈中性: 2H++SO42﹣+Ba2++2OH﹣=BaSO4↓+2H2O | NaHSO4溶液与Ba(OH)2溶液反应呈中性: 2H++SO42﹣+Ba++2OH﹣=BaSO4↓+2H2O |
C | 铁和氯气反应2Fe+3Cl2 | 铁和单质反应2Fe+3I2 |
D | 向Ca(ClO)2溶液中通入少量CO2: Ca2++2ClO﹣+CO2+H2O=CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2: Ca2++2ClO﹣+SO2+H2O=CaSO3↓+2HClO |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种化合物,均含有常见元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
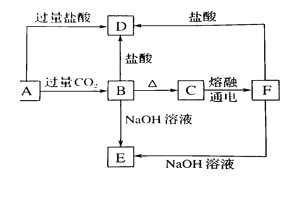
(1)写出化学式;
A______ ,C______ ,D______ ,E______
(2)写出下列反应的离子方程式:
①A→B: _____________________________________________
②B→E: _____________________________________________
③C→E: _____________________________________________
④F→E: _____________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理利用资源成为当今研究热点。CH3NH2、PbI2及HI常用作合成太阳能电池的敏化剂甲胺铅碘(CH3NH3PbI3)的主要原料。
(1)制取甲胺的反应为CH3OH(g)+NH3(g)![]() CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
共价键 | C-O | H-O | N-H | C-N |
键能/kJ·mol-1 | E1 | E2 | E3 | E4 |
则上述热化学方程式中ΔH=___kJ·mol-1。
(2)可利用水煤气合成上述反应所需甲醇。反应为CO(g)+2H2(g)![]() CH3OH(g)ΔH<0。在一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
CH3OH(g)ΔH<0。在一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
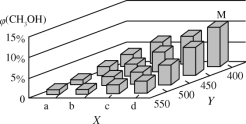
①平衡时,M点CH3OH的体积分数为10%,则CO的转化率为___。
②图中Y轴表示温度,其判断的理由是__。
(3)可利用四氧化三铅和氢碘酸反应制备难溶PbI2,若反应中生成amolPbI2,则转移电子的物质的量为___。
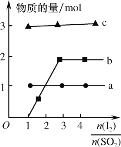
(4)将二氧化硫通入碘水制备HI的反应曲线如图所示,其反应原理为:SO2+I2+2H2O=3H++HSO4-+2I-,I2+I-![]() I3-,图中曲线a、b分别代表的微粒是__和__(填微粒符号);由图知要提高碘的还原率,除控制温度外,还可以采取的措施是___。
I3-,图中曲线a、b分别代表的微粒是__和__(填微粒符号);由图知要提高碘的还原率,除控制温度外,还可以采取的措施是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡酸钠晶体(Na2SnO33H2O2)在染料工业用作媒染剂。以锡渣废料(主要成分是SnO,还含有少量Fe、Te、Sb、Pb、As等元素的氧化物)为原料,制备锡酸钠晶体的工艺流程图如图:
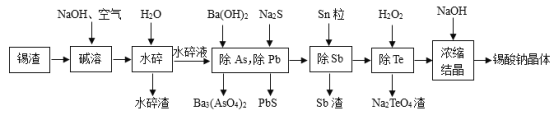
已知:水碎液中溶质的主要成分为Na2SnO3、Na3AsO4、Na3SbO4、Na2PbO2、Na2TeO3。
(1)“碱溶”时,SnO发生反应的化学方程式为___。
(2)工业上制备锡酸钠晶体(Na2SnO33H2O)时,会将“水碎渣”再次水洗,其目的是___。
(3) “除Sb”时发生反应的离子方程式为___。
(4) “除Te”过程中氧化剂与还原剂的物质的量之比为___,该过程中反应时间、反应温度对Te的脱除率的影响关系如图,则70℃后随温度升高Te的脱除率下降的原因可能是___;“除Te”的最优反应时间和反应温度分别为___、___。
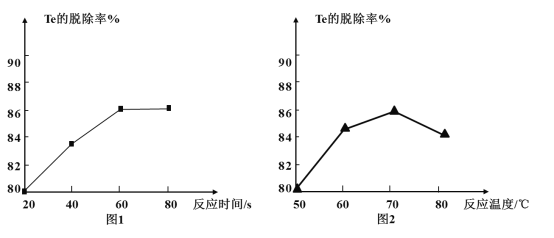
(5)已知锡酸钠的溶解度一般随着温度的升高而升高,则在“浓缩、结晶”时,加入NaOH的原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M的结构如图所示,X、Y、Z、W是原子序数依次增大的短周期主族元素,其中W的核外电子数是Y的两倍。下列说法正确的是( )
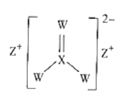
A.简单离子的半径:W>Z>Y
B.最简单氢化物的沸点:W>X>Y
C.Y、W均能和Z形成两种化合物
D.W的单质不能溶于XW2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知G、Q、X、Y、Z均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):
①G―→Q+NaCl ②Q+H2O![]() X+H2
X+H2
③Y+NaOH―→G+Q+H2O
④Z+NaOH―→Q+X+H2O
这五种化合物中Cl元素化合价由低到高的顺序是( )
A. G、Y、Q、Z、X B. X、Z、Q、G、Y
C. X、Z、Q、Y、G D. G、Q、Y、Z、X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com