
【题目】有机物的结构简式可进一步简化,如:
CH3CH2CH2CH3: 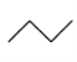 ,
,![]() :
: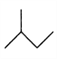 ,CH3CH=CHCH3 :
,CH3CH=CHCH3 :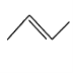
(1)写出下列有机物的结构简式:
2,2,3,3-四甲基戊烷:____________________;
3,4-二甲基-4-乙基庚烷:____________________。
(2)写出下列物质的分子式:
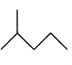 :__________________________;
:__________________________;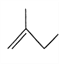 :__________________________。
:__________________________。
(3)用系统命名法命名下列物质:
![]() ____________________。
____________________。
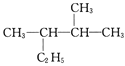 ____________________。
____________________。
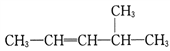 ____________________。
____________________。
![]() ____________________。
____________________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】[选修5:有机化学基础]扁桃酸衍生物是重要的医药中间体,以A和B为原料合成扁桃酸衍生物F的路线如下:
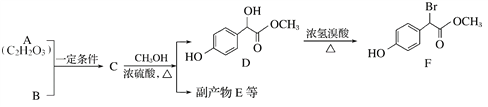
(1)A可发生银镜反应,且具有酸性,A的结构简式为____________。B的分子式为C6H6O,则A与B所发生反应的类型为___________。
(2)C生成D的化学方程式为_____________________________。E是由2分子C生成的含有3个六元环的化合物,E的结构简式为______________。
(3)1 mol F在一定条件下与足量NaOH溶液反应,最多消耗NaOH的物质的量为_______mol。符合下列条件的F的同分异构体(不考虑立体异构)共有______种。
①苯环上只有2个取代基且处于对位,其中一个是羟基;
②在稀H2SO4中或NaOH溶液中加热均能发生水解反应;
③能发生银镜反应。
(4)已知:R—CH2—COOH![]()
![]() ,A有多种合成方法,在下面的空格处写出由乙酸合成A的路线流程图(其他原料任选)。合成路线流程图示例如下:
,A有多种合成方法,在下面的空格处写出由乙酸合成A的路线流程图(其他原料任选)。合成路线流程图示例如下:
H2C===CH2![]() CH3CH2OH
CH3CH2OH![]() CH3COOC2H5
CH3COOC2H5
_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类、油脂、蛋白质都是人类重要的营养物质。回答下列问题:
(1)淀粉和纤维素是两种重要的多糖,这两种物质________(填“能”或“不能”互称为同分异构体,淀粉完全水解的化学方程式为______________。
(2)在常温常圧下、油脂既有呈固态的,也有呈液态的。某液态油脂的一种成分的结构简式为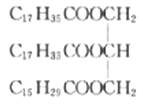 ,则该油脂______(填“能”或“不能”)使溴水褪色,该油脂在热NaOH溶液中水解的产物有C17H35COONa、C17H33COONa、_____________。
,则该油脂______(填“能”或“不能”)使溴水褪色,该油脂在热NaOH溶液中水解的产物有C17H35COONa、C17H33COONa、_____________。
(3)发育出现障碍,患背养缺乏症,这主要是由摄入蛋白质不足引起的。蛋白质在人体内水解的最终产物是_______;向蛋白质溶液中加入(CH3COO)2Pb溶液会出现白色沉淀,该变化叫作_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是一种纯净的无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
实验步骤 | 解释或实验结论 |
称取A物质27.0g,升温使其汽化,测其密度是相同条件下NO的3倍 | (1)A的相对分子质量为:____________ |
(2)A的核磁共振氢谱如图:
| (2)A中含有______种氢原子 |
(3)另取A27.0g与足量的NaHCO3粉末反应,生成0.3molCO2,若与足量钠反应则生成0.3mol H2 | (3)写出A中所含官能团的名称:___________ |
(4)将此27.0gA在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者依次增重16.2g和39.6g | (4)A的分子式为:________ |
(5)综上所述A的结构简式为:_______________________________ | |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向1L 0.4mol/L HN03溶液中加入Fe粉和Cu粉的混合物9g,充分反应,放出NO气体且金属有剩余。则反应后溶液中c(NO3-)为(忽略溶液体积的变化)
A. 0. 2mol/L B. 0.225 mol/L C. 0.3mol/L D. 0.325 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z组成的化合物Y2X和ZX2。Y2X溶于水形成的溶液能与ZX2反应生成一种化合物Y2ZX3。已知三种元素原子的质子总数为25,且Z和Y的原子序数之和比X的原子序数2倍还多1,Z原子的最外层电子数是次外层电子数的2倍。试回答:
(1)X、Y、Z元素的名称及符号_________、___________、____________。
(2)写出ZX2的化学式______________。
(3)写出Y2X对应水化物的电子式_________,并指出其中存在的化学键___________________。
(4)写出Y2X溶于水的溶液与ZX2反应的化学方程式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
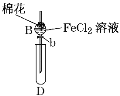
Ⅰ.先向B中的FeCl2溶液(约10mL)中通入Cl2,当B中溶液变黄时,停止通气。
Ⅱ.打开活塞b,使约2mL的溶液流入D试管中,检验取出溶液中的离子。
Ⅲ.接着再向B中通入一定量的SO2气体。
Ⅳ.更新试管D,重复过程Ⅱ,检验取出溶液中的离子。
(1)棉花中浸润的溶液为____________,目的是________________。
(2)实验室制备氯气的化学方程式为______________________。
(3)过程Ⅲ中一定发生反应的离子方程式为______________________,过程Ⅳ中检验取出溶液中是否含有硫酸根的操作是_____________________。
(4)该小组对SO2、Fe2+和Cl-还原性强弱比较期望达到的结论是_______________。
(5)甲、乙、丙三同学分别完成了上述实验,下表是他们的检测结果,他们的检测结果一定能够证明SO2、Fe2+和Cl-还原性强弱关系的是______________。
过程Ⅱ中检出离子 | 过程Ⅳ中检出离子 | |
甲 | 有Fe3+无Fe2+ | 有SO42- |
乙 | 既有Fe3+又有Fe2+ | 有SO42- |
丙 | 有Fe3+无Fe2+ | 有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用98%的浓硫酸(ρ=1.84g/cm3)配制1mol/L稀硫酸100mL.
(1)实验操作:
a.用100mL量筒量取98%的浓硫酸___________mL;
b.选取对应规格的容量瓶,洗涤,检查是否漏液,将稀释并冷却至室温的硫酸溶液沿玻璃棒转移到此容量瓶中;
c.用少量蒸馏水洗涤小烧杯和玻璃棒2--3次,并将洗涤液转移到容量瓶中;
d.在小烧杯内稀释浓硫酸,稀释时要用玻璃棒不断搅拌;
e.向容量瓶中直接加蒸馏水至离刻度线1---2cm处;
f.盖上容量瓶瓶塞,摇匀;
g.用胶头滴管小心加蒸馏水至刻度线;
h.将配制好的溶液转移入含少量蒸馏水的试剂瓶中贮存备用.
(2)实验分析:
①正确的操作步骤是__________________________________________________(填序号).
②此实验中玻璃棒的作用是__________________________________________________.
③实验操作中有两处错误,这两处错误是:
I.____________________________________________________________Ⅱ._____________________________________________.
(3)下列操作对所配溶液的浓度有何影响?(填“偏高”“偏低”或“无影响”)
I.量取浓硫酸的量筒用蒸馏水洗涤两次,并将洗涤液转入容量瓶中______________.
II.定容时俯视容量瓶刻度线__________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com