
| A. | 离子键 | B. | 金属键 | C. | 氢键 | D. | 配位键 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
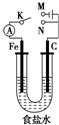
| A. | 若电键K与N连接,铁被保护不会腐蚀 | |
| B. | 若电键K与M连接,将石墨棒换成铜棒,可实现铁棒上镀铜 | |
| C. | 若电键K与N连接,正极反应式是 4OH--4e-═2H2O+O2↑ | |
| D. | 若电键K与M连接,当两极共产生22.4L(标准状况)气体时,生成了1mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X2+>R2+>Y2+>Z2+ | B. | Y2+>Z2+>R2+>X2+ | C. | Z2+>X2+>R2+>Y2+ | D. | R2+>X2+>Z2+>Y2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在一密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,如图表示该反应的速率(v)在某一时间段内的变化.则下列时间段中,SO3的百分含量最高的是( )
在一密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,如图表示该反应的速率(v)在某一时间段内的变化.则下列时间段中,SO3的百分含量最高的是( )| A. | t0→t1 | B. | t2→t3 | C. | t3→t4 | D. | t3→t5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
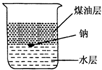
| A. | 钠在水层中反应并四处游动 | |
| B. | 钠停留在煤油层中不发生反应 | |
| C. | 钠在煤油的液面上反应并四处游动 | |
| D. | 钠在水与煤油的界面处反应并上下跳动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
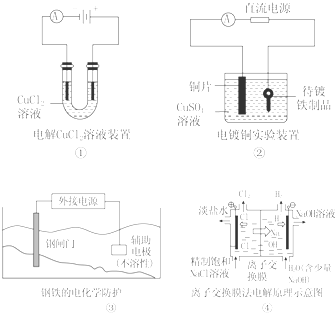
| A. | ①中阴极处能产生使湿润淀粉KI试纸变蓝的气体 | |
| B. | ②中待镀铁制品应与电源正极相连 | |
| C. | ③中钢闸门应与外接电源的正极相连 | |
| D. | ④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
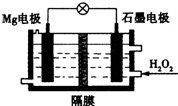 Mg-H2O2电池可用于驱动无人驾驶潜航器.该电池以海水为电解质溶液,示意如图.该电池工作时,下列不正确的是( )
Mg-H2O2电池可用于驱动无人驾驶潜航器.该电池以海水为电解质溶液,示意如图.该电池工作时,下列不正确的是( )| A. | Mg电极是该电池的负极 | B. | H2O2在石墨电极上发生还原反应 | ||
| C. | 石墨电极附近溶液的pH减小 | D. | 溶液中Cl-向负极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
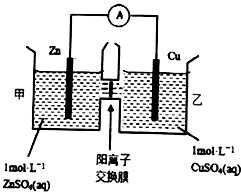
| A. | 铜电极上发生还原反应 | |
| B. | 电池工作一段时间后,甲池的c(SO42-)减小 | |
| C. | 电池工作一段时间后,乙池溶液的总质量不变 | |
| D. | 阳离子通过交换膜向正极移动,保持溶液中电荷平衡 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com