
| A.2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
| B.I2+SO2+2H2O=H2SO4+2HI |
| C.SO2+2Cl-+2H2O=S↓+Cl2↑+4OH- |
| D.2Fe3++2I-=2Fe2++I2 |
科目:高中化学 来源:不详 题型:单选题
| A.Na2CO3+CaCl2=CaCO3↓+2NaCl |
| B.2Cu+O2=2CuO |
| C.CaCO3+2HCl=H2O+CO2↑+CaCl2 |
| D.2H2+O2=2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓H2SO4>Br2>Fe3+>Cu2+ |
| B.浓H2SO4>Cu2+>Fe3+>Br2 |
| C.Br2>浓H2SO4>Fe3+>Cu2+ |
| D.Fe3+>Cu2+>Br2>浓H2SO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2NaW+Z2=2NaZ+W2 | B.2NaZ+Y2=2NaY+Z2 |
| C.2NaY+W2=2NaW+Y2 | D.2NaZ+X2=2NaX+Z2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.I-具有氧化性 | B.Cl2是还原剂 |
| C.该反应属于置换反应 | D.氯气的氧化性比碘强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cl2>Fe3+>Cu2+ | B.Fe3+>Cl2>Cu2+ |
| C.Cu2+>Fe3+>Cl2 | D.Cl2>Cu2+>Fe3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


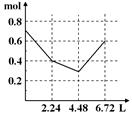

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.测0.1mol/L氨水的pH为11:NH3·H2O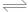 NH4++OH- NH4++OH- |
| B.将Na块放入水中,产生气体:2Na+2H2O=2NaOH+H2↑ |
C.用CuCl2溶液做导电实验,灯泡发光:CuCl2 Cu2++2Cl- Cu2++2Cl- |
| D.Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2Na2O2+2H2O===4NaOH+O2↑ | B.2F2+2H2O===4HF+O2 |
| C.2Na+2H2O===2NaOH+H2↑ | D.NaH+H2O===NaOH+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com