
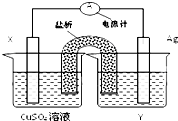
 依据氧化还原反应2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示:
依据氧化还原反应2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示:

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、人类历史上使用最早的合金是青铜 |
| B、合金的熔点比它的各成分金属的熔点都低 |
| C、合金中不一定含有金属 |
| D、目前世界上用途最广泛的合金是钢 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、需要加热的化学反应都是吸热反应 |
| B、原电池是将电能转化为化学能的一种装置 |
| C、物质的燃烧都是放热反应 |
| D、化学键的形成需吸收能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2:3 | B、3:2 |
| C、2:5 | D、1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、15g乙烷所含极性共价键的数目为3NA |
| B、0.1mol 甲基含有的质子数6.02NA |
| C、常温下,100mL0.1mol/L醋酸溶液中含醋酸分子为0.01NA |
| D、0.5mol乙醇完全燃烧时,转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、粘附在试管壁上的硫可用二硫化碳清洗 |
| B、S2和S8是同素异形体 |
| C、硫在自然界中主要以化合态形式存在 |
| D、硫粉和铜粉混合共热生成黑色的CuS |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com