



科目:高中化学 来源: 题型:
| 用途或现象 | 体现浓硫酸的性质 |
| (1)浓硫酸使胆矾由蓝色变成白色 | |
| (2)将浓硫酸滴在一张纸片上发现纸片变黑. | |
| (3)铜与浓硫酸加热,溶液变蓝并产生有刺激性气味的气体 | |
| (4)浓硫酸作为干燥剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
35 17 |
37 17 |
 与
与  ⑥CH3-CH2-OH和CH3-O-CH3
⑥CH3-CH2-OH和CH3-O-CH3查看答案和解析>>
科目:高中化学 来源: 题型:
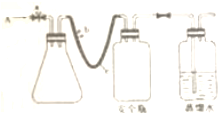 实验室用下列方法测定某水样中O2的含量
实验室用下列方法测定某水样中O2的含量2- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 温度 | H2O2溶液初始浓度 | MnO2颗粒大小 |
| 1 | 25℃ | 4% | 无MnO2 |
| 2 | 25℃ | 12% | 1g细颗粒MnO2 |
| 3 | 25℃ | 4% | 1g细颗粒MnO2 |
| 4 | 25℃ | 4% | 1g粗颗粒MnO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、氯原子的结构示意图: | ||
B、H2O分子的比例模型: | ||
C、作为相对原子质量测定标准的碳核素:
| ||
D、用电子式表示氯化氢分子的形成过程: |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下“纳米铜”比铜片的还原性强,反应时反应速率快 |
| B、“纳米铜”颗粒更细小,化学反应时接触面大,所以反应速率快 |
| C、“纳米铜”与铜是同素异形体 |
| D、常温下“纳米铜”比铜片更易得电子,反应时反应速率快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 相对分子质量为174的有机物M中只含有C、H、O三种元素,其分子结构如图所示.请回答下列问题:
相对分子质量为174的有机物M中只含有C、H、O三种元素,其分子结构如图所示.请回答下列问题: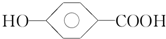 ,该反应的化学方程式是
,该反应的化学方程式是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com