
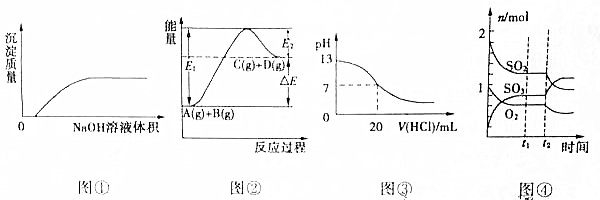
| A. | 图①表示将NaOH溶液滴入Ba(HCO3)2溶液中 | |
| B. | 图②表示反应物的总键能小于生成物的总键能 | |
| C. | 图③表示25℃时,0.1mol/L盐酸滴入20mL0.1mol/LNaOH溶液中,溶液的pH随加入酸体积的变化曲线 | |
| D. | 图④表示一定条件下的反应2SO2(g)+O2?2SO3(g)△H<0,t2时刻改变的曲线 |
分析 A.氢氧化钠与碳酸氢钡反应生成碳酸钡和碳酸钠;
B.图②表示反应物总能量低于生成物总能量,为吸热反应;
C.20mL0.1mol/LNaOH溶液PH为13,加入盐酸发生反应生成氯化钠,1mol盐酸消耗1mol氢氧化钠据此解答;
D.反应中转化量之比等于计量系数之比;
解答 解:A.氢氧化钠与碳酸氢钡反应生成碳酸钡和碳酸钠,加入氢氧化钠立刻产生沉淀,故A错误;
B.图②表示反应物总能量低于生成物总能量,为吸热反应,吸热反应断键吸收能量大于成键释放能量,故B错误;
C.20mL0.1mol/LNaOH溶液PH为13,加入盐酸发生反应生成氯化钠,1mol盐酸消耗1mol氢氧化钠,当加入0.1mol/L盐酸20mL,恰好中和,溶液呈中性,继续滴加盐酸,溶液显酸性pH减小,故C正确;
D.由图④可知时,0-t1时,二氧化硫、三氧化硫变化量为3mol,氧气变化量为2mol,二氧化硫、氧气、三氧化硫三者转化量之比为3:2:3,与方程式计量系数不成比例,故D错误;
故选:C.
点评 本题为图象题,明确物质之间发生的反应,反应热效应与反应物、生成物总能量之间的关系、影响平衡的因素是解题关键,题目难度中等.


科目:高中化学 来源: 题型:填空题
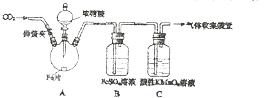 甲、乙两同学用如图所示装置进行实验,探究硝酸与铁反应的产物.
甲、乙两同学用如图所示装置进行实验,探究硝酸与铁反应的产物.| 实验操作 | 实验现象 |
| 打开弹簧夹,通入一段时间CO2,关闭弹簧夹. | / |
| 打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞. | 无明显现象. |
| 加热烧瓶,反应开始后停止加热. | ①A中有红棕色气体产生,一段时间后,气体颜色逐渐变浅; B中溶液变棕色; C中溶液紫色变浅. ②反应停止后,A中无固体剩余 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| A | |||||||
| B | C | D | |||||
| E | F | G | H | I | |||
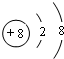 ,E与I形成的化合物的电子式为
,E与I形成的化合物的电子式为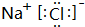 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 此混合气体中可能含有乙烷 | |
| B. | 此气体中一定含有甲烷 | |
| C. | 此混合气体中一定不含有丙烷 | |
| D. | 此气体若是乙烯与甲烷的混合气体,则甲烷与乙烯的体积比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| H | Z |
| A. | 常温下,含H的两种离子都能使水电离出的c•(H+)•c(OH-)增大 | |
| B. | Y的简单氢化物和Y的最高价含氧酸之间能发生氧化还原反应 | |
| C. | X的气态氢化物的热稳定性比Y的气态氢化物的热稳定性强 | |
| D. | 简单离子半径的大小顺序为H>Z>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
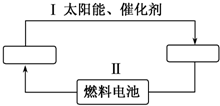 能源是21世纪极具发展前景的新能源之一,它既是绿色能源,又可循环使用.
能源是21世纪极具发展前景的新能源之一,它既是绿色能源,又可循环使用.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干冰升华,克服的是CO2的分子间作用力 | |
| B. | 碳原子间连接方式的多样性,是含碳化合物种类繁多的原因之一 | |
| C. | 在N2、CO2和SiO2物质中,都存在共价键,它们都是由分子构成 | |
| D. | NH4Cl属于离子化合物,该物质中存在离子键和共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com