
| A. | 与氢氧化钠溶液反应 | B. | 使溴的四氯化碳溶液褪色 | ||
| C. | 与金属钠反应放出氢气 | D. | 使高锰酸钾溶液褪色 |
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 19 | B. | 18 | C. | 27 | D. | 9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
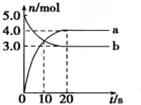
| A. | 曲线a表示NO2的物质的量随时间的变化 | |
| B. | 10s时,v(正)>v(逆) | |
| C. | 20s时反应达到平衡 | |
| D. | 0~20s内平均反应速率v(O2)=0.05mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X是正极 | B. | Y是正极 | ||
| C. | Y极发生还原反应 | D. | 电子由X极移向Y极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3C18OOH与C2H518OH | B. | CH3C18O18OH与C2H518OH | ||
| C. | CH3CO18OH与C2H518OH | D. | CH3CO18OH 与C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷和丙烯的物质的量共1mol,完全燃烧可生成3molH2O | |
| B. | 等质量的乙烯与聚乙烯完全燃烧,产生的CO2质量相等 | |
| C. | 乙醇和乙醚互为同分异构体 | |
| D. | 用水可区分苯和四氯化碳 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com