
| A. | O2->F->Na+>Mg2+ | B. | Na>Mg>Cl>Ar | C. | I>Br>F>Cl | D. | Na>Na+>S2->S |
分析 粒子的电子层越多,粒子半径越大,电子层相同时,粒子的核电荷数越大,离子半径越小;当核电荷数、核外电子层数都相等时,核外电子总数越多,微粒半径越大,注意同一周期中稀有气体的原子半径较大,据此进行解答.
解答 解:A.四种离子的电子层相同,核电荷数越大,离子半径越小,则离子半径大小为:O2->F->Na+>Mg2+,故A正确;
B.同一周期中,稀有气体的原子半径较大,则Ar的原子半径大于Na,故B错误;
C.同一主族元素,核电荷数越大,原子半径越小,则原子半径:I>Br>Cl>F,故C错误;
D.Na+的电子层最少,其离子半径最小,Na、S2-、S的核外电子层数都是3,核电荷数越大,微粒半径越小;当核电荷数、电子层相同时,核外电子总数越多,微粒半径越大,则微粒半径大小为:Na>S2->S>Na+,故D错误;
故选A.
点评 本题考查了元素周期律内容的综合应用,题目难度不大,试题侧重考查微粒半径大小比较,明确粒子比较大小规律为解答关键,试题培养了学生的灵活应用能力.


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌粒与稀硫酸的反应 | |
| B. | 灼热的木炭与CO2反应 | |
| C. | 甲烷在氧气中的燃烧反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜基态原子核外电子排布式为1s22s22p63s23p64s13d10 | |
| B. | 在d轨道中电子排布成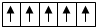 而不是 而不是 ,其最直接的根据是泡利原理 ,其最直接的根据是泡利原理 | |
| C. | 下列轨道的能量是按由高到低排列的E5s>E4s>E3d>E2p>E1s | |
| D. | 焰色反应、激光、霓虹灯光等与原子核外电子发生跃迁释放能量有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
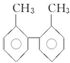
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.288g | B. | 0.366g | C. | 0.384g | D. | 0.396g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com