
| y |
| 4 |
| 4 |
| 4 |
| 4 |
| 4 |
| 6 |
| 4 |


科目:高中化学 来源: 题型:
| A、④⑤⑨ | B、⑦⑧⑩ |
| C、①②③⑨ | D、②⑦⑨⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:
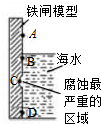 铁及其化合物与生产、生活关系密切.
铁及其化合物与生产、生活关系密切.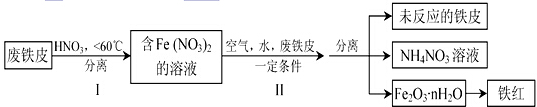
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用热的纯碱溶液洗涤粘有油脂的餐具 |
| B、用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验 |
| C、用米汤检验食用加碘盐(含KIO3)中含有碘 |
| D、用灼烧方法鉴别羊毛布料和纯棉布料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com