
| A. | 等于0.6mol | B. | 等于0.15mol | ||
| C. | 介于0.15mol与0.3mol之间 | D. | 等于0.3mol |
分析 由于Cu足量,则浓硝酸完全反应,被还原的硝酸生成NO2、NO,由N元素守恒可知:2n[Cu(NO3)2]+n(气体)=n(HNO3)=0.05L×12mol/L=0.6mol,生成气体只有NO2时,被还原的硝酸达极大值,只有NO时,被还原的硝酸到极小值,再结合电子转移守恒计算.
解答 解:由于Cu足量,则浓硝酸完全反应,反应生成气体为NO2、NO,由N元素守恒可知:2n[Cu(NO3)2]+n(气体)=n(HNO3)=0.05L×12mol/L=0.6mol,
生成气体只有NO2时,被还原的硝酸达极大值,根据电子转移守恒2n[Cu(NO3)2]=n(NO2),联立方程解得:n(NO2)=0.3mol;
只有NO时,被还原的硝酸到极小值,根据电子转移守恒2n[Cu(NO3)2]=3n(NO),联立方程解得:n(NO)=0.15mol,
由N原子守恒被还原的硝酸介于0.15mol与0.3mol之间,
故选:C.
点评 本题考查硝酸性质、化学计算,侧重考查学生分析计算能力,注意守恒法与极限法应用.


科目:高中化学 来源: 题型:选择题
| A. | 1-丙醇制丙烯;丙烯与溴水反应制1,2-二溴丙烷 | |
| B. | 溴乙烷水解制丙醇;丙烯与水反应制丙醇 | |
| C. | 甲苯硝化制对硝基甲苯;甲苯氧化制苯甲酸 | |
| D. | 乙酸和乙醇制乙酸乙酯;苯甲酸乙酯水解制苯甲酸和乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
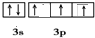 .
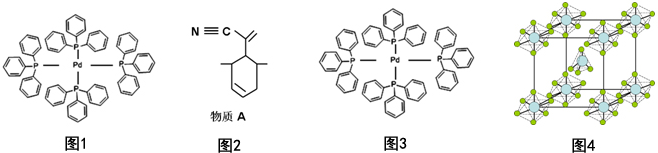
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用碱式滴定管量取25.03mLH2SO4溶液 | |
| B. | 用50mL量筒量取21.48mL稀硫酸 | |
| C. | 用pH试纸测定HNO3溶液的pH=3.7 | |
| D. | 用托盘天平称取11.7gNaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:l | B. | 1:2 | C. | 3:2 | D. | 2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜能导电,所以铜是电解质 | |
| B. | BaSO4难溶于水,所以BaSO4属于非电解质 | |
| C. | 虽然液态HCl不能导电,但HCl的水溶液能导电,所以HCl是电解质 | |
| D. | 氯气的水溶液能导电,氯气是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有②③ | C. | 全部 | D. | 只有③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在船舶的外壳装上镁合金或锌块保护钢铁设备被称为牺牲阳极的阴极保护法 | |
| B. | 赤潮、白色污染、绿色食品中的“赤”“白”“绿”均指相关物质的颜色 | |
| C. | 海水淡化的方法主要有:蒸馏法、电渗析法、离子交换法等 | |
| D. | 乙烯的产量可以用来衡量一个国家的石油化工发展水平 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO4在熔融状态下的电离方程式为NaHSO4═Na++H++SO42- | |
| B. | H2CO3是弱酸,故Na2CO3是弱电解质 | |
| C. | Fe3O4俗称铁红,常用作红色油漆和涂料 | |
| D. | 2.4 g Mg无论与O2还是与N2完全反应转移的电子数均为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com