

分析 A和浓盐酸在加热条件下反应生成黄绿色气体D,则D为Cl2,A应为MnO2,生成的E为MnCl2溶液,MnO2和KOH与氧气在熔融状态下反应生成K2MnO4和H2O,K2MnO4在酸性条件下自身发生氧化还原反应生成KMnO4和MnO2,则B为K2MnO4,C为KMnO4,KMnO4不稳定,加热生成K2MnO4、MnO2和O2,则F为O2,以此解答该题.
解答 解:A和浓盐酸在加热条件下反应生成黄绿色气体D,则D为Cl2,A应为MnO2,生成的E为MnCl2溶液,MnO2和KOH与氧气在熔融状态下反应生成K2MnO4和H2O,K2MnO4在酸性条件下自身发生氧化还原反应生成KMnO4和MnO2,则B为K2MnO4,C为KMnO4,KMnO4不稳定,加热生成K2MnO4、MnO2和O2,则F为O2,
(1)C为KMnO4,KMnO4不稳定,加热生成K2MnO4、MnO2和O2,反应的方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,
A为MnO2,可与氧气在碱性条件下反应生成锰酸钾,方程式为2MnO2+4KOH+O2$\frac{\underline{\;\;△\;\;}}{\;}$2K2MnO4+2H2O,
故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;2MnO2+4KOH+O2$\frac{\underline{\;\;△\;\;}}{\;}$2K2MnO4+2H2O;
(2)MnO2和浓盐酸在加热条件下反应生成黄绿色气体Cl2和MnCl2溶液,反应的离子方程式为MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
K2MnO4在酸性条件下自身发生氧化还原反应生成KMnO4和MnO2,反应的离子方程式为3MnO4-+4H+=2MnO4-+MnO2↓+2H2O,
故答案为:MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;3MnO42-+4H+=2MnO4-+MnO2↓+2H2O.
点评 本题考查无机物的推断和氯气的性质,为高频考点,侧重学生的分析能力和元素化合物知识的综合理解和运用的考查,题目难度中等,本题注意把握KMnO4、K2MnO4、MnO2等物质的性质.


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
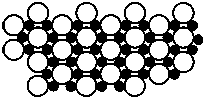 2001年3月发现硼化镁在39K时呈超导性,可 能是人类对超导认识的新里程碑.在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼的相间排列,如图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上.根据下图确定硼化镁的化学式为( )
2001年3月发现硼化镁在39K时呈超导性,可 能是人类对超导认识的新里程碑.在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼的相间排列,如图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上.根据下图确定硼化镁的化学式为( )| A. | MgB | B. | MgB2 | C. | Mg2B | D. | MgB6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 原子半径:Y>Z>X | |
| B. | 若Y的氧化物为两性氧化物,则Z的一种单质在空气中易自燃 | |
| C. | 若X的气态氢化物与Z的最高价氧化物的水化物能反应,则生成的盐仅有一种 | |
| D. | 若Y与Z的核电荷数之和为X的4倍,则X、Y、Z的氢化物分子的立体构型分别为:V形,三角锥形,直线形 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
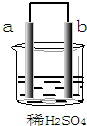
| A. | b极上发生了还原反应 | |
| B. | a是正极,b是负极 | |
| C. | a极上放出气体,溶液的pH增大 | |
| D. | 导线中有电子流动,电子从b极流到a极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1+3Q2>6Q3 | B. | Q1+3Q2<6Q3 | C. | Q1+Q2<Q3 | D. | Q1+Q2=Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:HClO4>HBrO4>HIO4 | B. | P、S、C1元素最高正价依次升高 | ||
| C. | 稳定性:PH3>H2S>HCl | D. | 离子半径:Mg2+<Na+<F- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电能转化为化学能 | B. | 电解质溶液是稀硫酸 | ||
| C. | 电子通过外电路从正极流向负极 | D. | Zn做负极被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com