
【题目】由乙烯和其他无机原料合成环状酯E和髙分子化合物H的示意图如图所示:
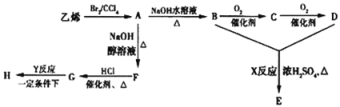
请回答下列问题:
(1)写出以下物质的结构简式:B______,G_______
(2)写出以下反应的反应类型:X_____,Y______.
(3)写出以下反应的化学方程式:A→B:_______
(4)若环状酯E与NaOH水溶液共热,则发生反应的化学方程式为______.
【答案】HOCH2CH2OH;CH2=CHCl 酯化反应 加聚反应 CH2BrCH2Br+2H2O![]() HOCH2CH2OH+2HBr; CH2OHCH2OH+HCCOC﹣COOH
HOCH2CH2OH+2HBr; CH2OHCH2OH+HCCOC﹣COOH![]()
![]() +2H2O
+2H2O ![]() +2NaOH
+2NaOH![]() NaOOCCOONa+HOCH2CH2OH
NaOOCCOONa+HOCH2CH2OH
【解析】
乙烯和溴发生加成反应生成A,A的结构简式为:CH2BrCH2Br,A和氢氧化钠的水溶液发生取代反应生成B,B的结构简式为:HOCH2CH2OH,B被氧气氧化生成C,C的结构简式为:OHC-CHO,C被氧气氧化生成D,D的结构简式为:HOOC-COOH,B和D发生酯化反应生成E,E是环状酯,则E乙二酸乙二酯;A和氢氧化钠的醇溶液发生消去反应生成F,F的结构简式为:HC≡CH,F和氯化氢发生加成反应生成G氯乙烯,氯乙烯发生加聚反应生成H聚氯乙烯。
根据以上分析,(1)B是乙二醇,B的结构简式为:HOCH2CH2OH,G氯乙烯,G的结构简式是CH2=CHCl;
(2)反应X是CH2OHCH2OH与HCCOC﹣COOH生成![]() ,反应类型是酯化反应;反应Y是CH2=CHCl 生成聚氯乙烯,反应类型是加聚反应;
,反应类型是酯化反应;反应Y是CH2=CHCl 生成聚氯乙烯,反应类型是加聚反应;
(3)CH2BrCH2Br和氢氧化钠的水溶液发生取代反应生成CH2OHCH2OH, 反应的化学方程式是CH2BrCH2Br+2H2O![]() HOCH2CH2OH+2HBr;
HOCH2CH2OH+2HBr;
(4)若环状酯E与NaOH水溶液共热发生水解反应,则发生反应的化学方程式为![]() +2NaOH
+2NaOH![]() NaOOCCOONa+HOCH2CH2OH。
NaOOCCOONa+HOCH2CH2OH。


科目:高中化学 来源: 题型:
【题目】为了验证浓硫酸和木炭粉在加热条件下产生的气体产物,某同学选用了如图所示的实验装置。下列说法错误的是

A. B装置用来检验产物中是否有水蒸气
B. 拆除E装置也能达到实验目的
C. F装置中出现白色浑浊证明产物中一定有CO2生成
D. C装置用来检验产物中是否有SO2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有N、P、Fe、Ti等元素的新型材料有着广泛的用途。
(1)基态Fe原子未成对电子数为______个;基态Ti原子的价电子排布图是_____________。
(2)意大利罗马大学的:FuNvio Cacace等人获得了极具理论研究意义的N4分子,其中氮原子的轨道杂化形式为__________________________。
(3)比较气态氢化物膦(PH3)和氨(NH3)的键角:PH3________NH3(填“大于”、“小于”或“等于”),主要原因为____________________________________________________________。
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如图所示。

①组成M的元素中,电负性最大的是___________(填名称)。
②M中含有_________(填标号)。
A π键 B σ键
C 离子键 D 配位键

(5)已知金刚石的晶胞沿其体对角线垂直在纸平面上的投影图如下图B所示,则金属铁晶胞沿其体对角线垂直在纸平面上的投影图应该是图__________(填标号)。

(6)某种磁性氮化铁的晶胞结构如图所示,其中距离铁原子最近的铁原子的个数为____________,氮化铁晶胞底边长为a cm,高为c cm,则这种磁性氮化铁的晶体密度为__________g·cm-3(用含a、c和NA的计算式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH是溶液中c(H+)的负对数,若定义pC是溶液中微粒物质的量浓度的负对数,则常温下,某浓度的草酸(H2C2O4)水溶液中pC(H2C2O4),pC(HC2O4-)、pC(C2O42-)随着溶液pH的变化曲线如图所示:下列说法不正确的是

A. 曲线I代表HC2O4-的浓度随着pH增大先变小后变大
B. 草酸的电离常数 Kal=l×10-1.3; Ka2= l×10-4.3
C. pH=4时,c(HC2O4-)>c(C2O42-)>c(H2C2O4)
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,圆底烧瓶中盛有 0.18g 镁条,加入 10.00mL2.00mol/L 的硫酸溶液 反应完全后,产生氢气 180mL。
(1)根据实验数据计算,气体的摩尔体积为_____。
(2)反应过程中,装置内空气没有排除,空气的体积对实验结果____(填“有”或“无”)影响,请简述理由:________
(3)有同学认为:若镁条中混有杂质,则实验结果会偏低。请列举实例分析该同学的观点是否正确?____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向50 mL溶有0.1molCl2的氯水中滴加2mol/L的NaOH溶液,得到溶液pH随所加NaOH溶液体积的变化图像如下图所示。下列说法正确的是

A. 若a点pH=4,且c(Cl-)=m·c(ClO-),则Ka(HClO)=![]()
B. 若x=100,b点对应溶液中:c(OH-)>c(H+),可用pH试纸测定其pH
C. b~c段,随NaOH溶液的滴入,![]() 逐渐增大
逐渐增大
D. 若y=200,c点对应溶液中:c(OH-)-c(H+)=2c(Cl-)+c(HClO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环戊烯是生产精细化工产品的重要中间体,其制备涉及的反应如下:
氢化反应: ,
,![]()
副反应: ,
,![]()
解聚反应: ,
,![]()
回答下列问题:
(1)反应![]() 的△H= _____ kJ/mol。
的△H= _____ kJ/mol。
(2)一定条件下,将环戊二烯溶于有机溶剂进行氢化反应(不考虑二聚反应),反应过程中保持氢气压力不变,测得环戊烯和环戊烷的产率(以环戊二烯为原料计)随时间变化如图所示:

①0~4h氢化反应速率比副反应快的可能原因是_________。
②最佳的反应时间为__h。若需迅速减慢甚至停止反应,可采取的措施有____(写一条即可)。
③一段时间后,环戊烯产率快速下降的原因可能是_________。
(3)解聚反应在刚性容器中进行(不考虑氢化反应和副反应)。
①其他条件不变,有利于提高双环戊二烯平衡转化率的是 ____(填标号)。
A.增大双环戊二烯的用量 B.使用催化剂 C.及时分离产物 D.适当提高温度
②实际生产中常通入水蒸气以降低双环戊二烯的温度(水蒸气不参与反应)。某温度下,通入总压为300 kPa的双环戊二烯和水蒸气,达到平衡后总压为500 kPa,双环戊二烯的转化率为80%,则p(H2O)=______kPa,平衡常数Kp=_______kPa (Kp为以分压表示的平衡常数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙苯是重要的化工原料,利用乙苯为初始原料合成高分子化合物J的流程如下图所示(部分产物及反应条件已略去):
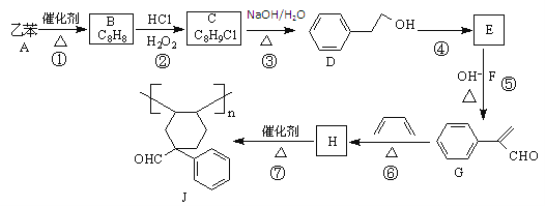
已知:①R1CHO+R2CH2CHO![]()
![]() +H2O
+H2O
②
(1)物质B的名称为________。反应④所需的试剂和条件分别为____。
(2)②、③的反应类型分别为_______。
(3)物质H中官能团的名称是_____;物质J的化学式是______。
(4)反应⑤的化学方程式为_____。
(5)写出符合下列条件,与G互为同分异构体的芳香族化合物的结构简式:_____。
ⅰ.与Na反应能够生成氢气;ⅱ.含碳碳叁键(不考虑“![]() ”结构);ⅲ.苯环上只有两个处于对位的取代基;ⅳ.核磁共振氢谱中峰的面积之比为2:2:2:1:1。
”结构);ⅲ.苯环上只有两个处于对位的取代基;ⅳ.核磁共振氢谱中峰的面积之比为2:2:2:1:1。
(6)参照上述合成路线和信息,设计由![]() 、乙醛、苯甲醇合成
、乙醛、苯甲醇合成 的路线_______(无机试剂任选)。
的路线_______(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中导电性最强的是( )
A. 1 L 0.1 mol/L AlCl3溶液 B. 0.1 L 0.1 mol/L H2SO4溶液
C. 0.5 L 0.15 mol/L盐酸 D. 2 L 0.1 mol/L H2SO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com