
【题目】I.(1)根据如图所示情况,判断下列说法中正确的是 。
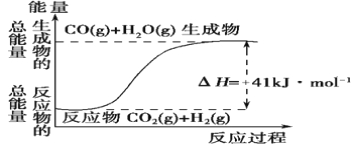
A.其热化学方程式为:CO(g)+ H2O(g)=CO2(g) + H2(g) ΔH=+41 kJ·mol-1
B.该反应为吸热反应
C.该反应为放热反应
D.若当H2O为液态时反应热为ΔH2,则ΔH2>ΔH
(2)25℃、101 kPa下,已知1g氢气完全燃烧生成液态水时放出142.9 kJ的热量,表示氢气燃烧热的热化学方程式是 。
(3)已知反应:N2(g) + O2 (g)=2NO(g) △H1
2H2(g)+ O2(g)=2H2O(g) △H2
N2(g)+3H2(g)=2NH3(g) △H3
利用上述三个反应,计算4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H4 的反应焓变为 (用含△H1、△H2、△H3的式子表示)。
(4)碘及其化合物在合成杀菌剂、药物等方面具有广泛用途.回答下列问题:已知反应2HI(g) ![]() H2(g)+I2(g) 的△H=+11kJmol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为 kJ。
H2(g)+I2(g) 的△H=+11kJmol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为 kJ。
【答案】
(1)B;
(2)H2(g)+0.5O2(g)=H2O(l) △H2=-285.8kJ·mol-1;
(3)2△H1+3△H2-2△H3;
(4)①MnO2+2I-+4H+=Mn2++I2+2H2O;②299。
【解析】
试题分析:(1)A、该反应热化学方程式为:CO2(g)+H2(g)=CO(g)+H2O(g)△H=41kJmol-1,故A错误;B、反应物能量小于生成物,正反应吸热,故B正确;C、正反应吸热,故C错误;D、水由气态变为液态放热,所以该反应吸热减少,其反应热的值小于41kJmol-1,故D错误;故答案为:B;
(2)1g氢气的物质的量为![]() =0.5mol,即0.5molH2完全燃烧生成液态水时放出142.9kJ的热量,则2molH2完全燃烧生成液态水时放出热量为142.9kJ×4=571.6kJ,则该反应的热化学方程式是2H2(g)+O2(g)=2H2O(1)△H=-571.6kJmol-1,故答案为:2H2(g)+O2(g)=2H2O(1) △H=-571.6kJmol-1;
=0.5mol,即0.5molH2完全燃烧生成液态水时放出142.9kJ的热量,则2molH2完全燃烧生成液态水时放出热量为142.9kJ×4=571.6kJ,则该反应的热化学方程式是2H2(g)+O2(g)=2H2O(1)△H=-571.6kJmol-1,故答案为:2H2(g)+O2(g)=2H2O(1) △H=-571.6kJmol-1;
(3)由①N2(g)+O2(g)═2NO(g)△H1,
②2H2(g)+O2(g)═2H2O(g)△H2,
③N2(g)+3H2(g)═2NH3(g)△H3,
结合盖斯定律可知,①×2+②×3-③×2
可得4NH3(g)+5O2(g)═4NO(g)+6H2O(g),则△H4=2△H1+3△H2-2△H3;
(4)①海藻中的碘元素以碘化物形式存在,反应中I元素发生氧化反应,Mn元素被还原,还原产物应为硫酸锰,反应的离子方程式为:2I-+MnO2+4H+=Mn2++I2+2H2O,故答案为:2I-+MnO2+4H+=Mn2++I2+2H2O;
②设1molHI(g)分子中化学键断裂时需吸收的能量为x kJ,则:2x kJ-436kJ-151kJ=11kJ,解得x=299,故答案为:299kJ。


科目:高中化学 来源: 题型:
【题目】中国丝绸有五千年的历史和文化,古代中国丝绸有五千年的历史和文化。古代染坊常用某种“碱剂”来精炼丝绸,该“碱剂”的主要成分是一种盐,能促进蚕丝表层的丝胶蛋白质水解而除去,使丝绸颜色洁白、质感柔软、色泽光亮。这种“碱剂”可能是
A. 食盐 B. 火碱 C. 草木灰 D. 胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国是世界上缺铁性贫血发生率较高的国家之一,2004年我国政府就已经启动了铁强化酱油项目,推广铁强化酱油.这里的铁是指( )
A. 元素 B. 单质
C. 原子 D. 分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种高能燃料,也广范应用在工业合成中。
(1)标准摩尔生成焓是指在25℃和101kPa,最稳定的单质生成1 mol化合物的焓变。已知25℃和101kPa时下列反应:
①2C2H6(g)+7O2(g)=4CO2(g)+6H2O(l) △H=-3116kJ·mol-1
②C(石墨,s)+O2(g)=CO2(g) △H=-393.5 kJ·mol-1
③2H2(g)+02(g)=2H2O(l),△H=-571.6 kJ·mol-1
写出乙烷标准生成焓的热化学方程式:_____________。
(2)已知合成氨的反应为:N2+3H2![]() 2NH3 △H <0。某温度下,若将1molN2和2.8molH2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:
2NH3 △H <0。某温度下,若将1molN2和2.8molH2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:

①图中代表反应在恒容绝热容器中进行的曲线是______(用a、b、c表示)。
②曲线a条件下该反应的平衡常数K=__________________。
③b容器中M点,v(正)_____ v(逆)(填“大于”、“小于”.或“等于”)。
(3)利用氨气可以设计成高能环保燃料电池,用该电池电解含有NO2-的碱性工业废水,在阴极产生N2。阴极电极反应式为_____;标准状况下,当阴极收集到1l.2LN2时,理论上消耗NH3的体积为_______。
(4)氨水是制备铜氨溶液的常用试剂,通过以下反应及数据来探究配制铜氨溶液的最佳途径。
已知:Cu(OH)2(s)![]() Cu2++2OH- Ksp=2.2×10-20
Cu2++2OH- Ksp=2.2×10-20
Cu2++4NH3·H2O![]() [Cu(NH3)4]2+(深蓝色)+4H2O Kβ=7.24×1012
[Cu(NH3)4]2+(深蓝色)+4H2O Kβ=7.24×1012
①请用数据说明利用该反应:Cu(OH)2(s)+4NH3·H2O![]() [Cu(NH3)4]2++4H2O+2OH- 配制铜氨溶液是否可行:________________。
[Cu(NH3)4]2++4H2O+2OH- 配制铜氨溶液是否可行:________________。
②已知反应Cu(OH)2(s)+2NH3·H2O+2NH4+![]() [Cu(NH3)4]2++4H2O K=5.16×102。向盛有少量Cu(OH)2固体的试管中加入14 mol/L的氨水,得到悬浊液;此时若加入适量的硫酸铵固体,出现的现象为__________;解释出现该现象的原因是_____________________。
[Cu(NH3)4]2++4H2O K=5.16×102。向盛有少量Cu(OH)2固体的试管中加入14 mol/L的氨水,得到悬浊液;此时若加入适量的硫酸铵固体,出现的现象为__________;解释出现该现象的原因是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+B===C+D,8g A和12g B恰好完全反应,生成C和9g D,则生成C的质量为( )
A. 9g B. 11g C. 10g D. 12g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧元素有三种核素16O、17O、18O,它们在自然界中所占的原子个数百分比分别为a%、b%、c%,则下列说法正确的是
A. 一个16O原子的质量为16 g
B. 17O的相对原子质量约为17
C. 氧元素的相对原子质量为![]()
D. 氧元素的相对原子质量为(16a%+17b%+18c%)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2SO2(g)+O2(g) ![]() 2SO3(g) △H=-197kJmol-1.向同温、同体积的三个密闭容器中分别充入气体:(甲) 2mol SO2和1mol O2;(乙) 1mol SO2和0.5mol O2;(丙) 2mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3(g) △H=-197kJmol-1.向同温、同体积的三个密闭容器中分别充入气体:(甲) 2mol SO2和1mol O2;(乙) 1mol SO2和0.5mol O2;(丙) 2mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是
A.容器内压强P:P甲=P丙>2P乙
B.SO3的质量m:m甲=m丙>2m乙
C.c(SO2)与c(O2)之比k:k甲=k丙>k乙
D.反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,X、Y、Z、W均为短周期元素,Z元素原子最外层电子数与电子总数之比为1∶3,则下列说法正确的是

A. 原子半径大小为W>Z>Y>X
B. W的最高价含氧酸的酸性最强
C. X、Z、Y、W的最髙正价分别为+4、+5、+6、+7
D. Z与W形成的所有化合物中.原子最外层电子均达到8e-稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氮的氧化物和一氧化碳在催化剂的作用下充分反应,生成氮气和二氧化碳。若测得氮气和二氧化碳的物质的量之比为1∶2,则该氮的氧化物是( )
A.N2O B.NO
C.NO2 D.N2O5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com