

| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Cu(OH)2 | 4.4 | 8.0 |
分析 (1)印刷电路板加入氯化铁溶液溶解铜,溶液中加入氧化剂氧化亚铁离子为铁离子,溶液中再加入氧化铜或氢氧化铜等调节溶液PH使铁离子全部沉淀,过滤得到滤液通过浓缩蒸发结晶析出,过滤洗涤得到氯化铜晶体,氯化氢气流中加热失去结晶水得到氯化铜固体;
①分析流程可知,步骤Ⅲ是过滤;
②加入试剂a能溶解铜,制备氯化铜,不能引入新的杂质;
③若不加入试剂b,溶液中亚铁离子不能除去,制备的氯化铜含有杂质;
(2)依据热化学方程式和盖斯定律计算得到所需热化学方程式;
(3)依据化学反应方程式,正极上是元素化合价降低,得到电子发生还原反应;
(4)用硝酸和硫酸共同浸泡印刷电路板制备硫酸铜,依据化学反应的定量关系计算得到.
解答 解:(1)印刷电路板加入氯化铁溶液溶解铜,溶液中加入氧化剂氧化亚铁离子为铁离子,溶液中再加入氧化铜或氢氧化铜等调节溶液PH使铁离子全部沉淀,过滤得到滤液通过浓缩蒸发结晶析出,过滤洗涤得到氯化铜晶体,氯化氢气流中加热失去结晶水得到氯化铜固体;
①分析流程可知,步骤Ⅲ是分离固体和溶液,用过滤操作,故答案为:过滤;
②加入试剂a能溶解铜,制备氯化铜,不能引入新的杂质;
A.HNO3溶液能溶解铜氧化亚铁离子,但引入硝酸根离子,故A错误;
B.Fe2(SO4)3溶液可以溶解铜,但会引入硫酸根离子,故B错误;
C.FeCl3溶液溶解铜,不引入新的杂质,故C正确;
故答案为:C;
③若不加入试剂b,溶液中亚铁离子不能除去,制备的氯化铜含有杂质,影响所得CuCl2纯度;
故答案为:否;不能除去Fe2+,影响所得CuCl2纯度;
(2)已知:①2H2O2(l)=2H2O (l)+O2(g)△H1=-196kJ/mol
②H2O(l)=H2(g)+1/2O2(g)△H2=+286kJ/mol
③Cu(s)+H2SO4(aq)=CuSO4(aq)+H2(g)△H3=+64kJ/mol
由盖斯定律①÷$\frac{1}{2}$-②+③得到:Cu(s)+H2O2(l)+H2SO4(aq)=CuSO4(aq)+2H2O(l)△H=-320kJ/mol,
故答案为:-320kJ/mol;
(3)正极上是元素化合价降低,得到电子发生还原反应,将反应Cu+H2O2+H2SO4=CuSO4+2H2O设计成原电池,是过氧化氢得到电子发生还原反应,其正极电极反应式是:H2O2+2H++2e-=2H2O,
故答案为:H2O2+2H++2e-=2H2O;
(4)用硝酸和硫酸共同浸泡印刷电路板制备硫酸铜,反应的化学方程式为3Cu+2HNO3+3H2SO4=3CuSO4+2NO↑+4H2O,欲制取3mol纯净的硫酸铜,依据化学方程式可知得到需要硝酸2mol,需要0.5mol/L的硝酸溶液的体积=$\frac{2mol}{0.5mol/L}$=4L,故答案为:4.
点评 本题考查了物质分离提纯流程的方法分析判断,试剂选择,热化学方程式书写,原电池原理的理解应用,注意化学方程式定量计算,掌握基础是解题关键,题目难度中等.


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:实验题

| 实验目的 | 操作 | 实验现象 | 结论 |
| 1.检验Cl- | 取少许滤液于试管中,加入硝酸酸化的硝酸银溶液 | 产生白色沉淀 | 含有Cl- |
| 2.检验NH4+ | 取少许滤液于试管中,加入浓氢氧化钠溶液并加热,将润湿的红色石蕊试纸置于试管口附近 | 石蕊试纸变蓝色 | 含有NH4+ k |
| 3.检验Zn2+ | 取少许滤液于试管中,加入稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
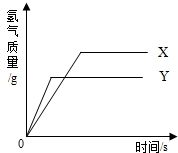 现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如右图所示(已知X、Y在生成物中化合价均为+2价).则下列说法中不正确的是( )
现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如右图所示(已知X、Y在生成物中化合价均为+2价).则下列说法中不正确的是( )| A. | 生成氢气的质量:X>Y | B. | 相对原子质量:X>Y | ||
| C. | 金属活动性:Y>X | D. | 消耗硫酸的质量:X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 质量比为11:8 | B. | 原子个数之比为2:3 | ||
| C. | 物质的量之比为3:2 | D. | 密度之比为8:11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 开发太阳能、水能、风能、可燃冰等新能源,减少使用煤、石油等化石燃料 | |
| B. | 将煤进行气化处理,提高煤的综合利用效率 | |
| C. | 研究采煤、采油新技术,提高产量以满足工业生产的快速发展 | |
| D. | 实现资源的“3R”利用观,即:减少资源消耗、增加资源的重复使用、资源的循环再生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火,可用泡沫灭火器扑灭 | |
| B. | 用10 mL量筒准确量取7.50 mL稀硫酸 | |
| C. | 用四氯化碳萃取溴水中的溴时,将溴的四氯化碳溶液从分液漏斗下口放出 | |
| D. | 在氢气还原氧化铜实验中,先加热氧化铜,后通入氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com