
| A. | 应用环形玻璃搅拌棒轻轻搅动混合液 | |
| B. | 实验中应使用相同浓度和体积的氢氧化钠溶液和盐酸溶液 | |
| C. | 实验中两个大小不同的烧杯间要填满碎纸条,目的是减少实验过程中热量的损失 | |
| D. | 用相同体积的浓硫酸代替盐酸溶液进行实验,测得中和热的数值比理论值偏高 |
分析 A.环形玻璃棒能上下搅拌液体,且不导热;
B.为保证盐酸完全反应,所加氢氧化钠应过量;
C.碎纸条能隔热;
D.浓硫酸稀释时放出热量.
解答 解:A.环形玻璃棒能上下搅拌液体,且不导热,所以使用环形玻璃棒既可以搅拌又避免损坏温度计,故A正确;
B.为保证盐酸完全反应,所加氢氧化钠应过量,NaOH溶液的体积与盐酸一样,但浓度稍大,故B错误;
C.因碎纸条能隔热,则烧杯间填满碎纸条是减少实验过程中的热量损失,故C正确;
D.浓硫酸稀释时放出热量,用相同体积的浓硫酸代替HCl溶液进行实验,放出的热量偏大,测得中和热的数值比理论值偏高,故D正确;
故选B.
点评 本题考查中和热的测定,明确实验装置及装置中各部分的作用、实验注意事项即可解答,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+ Na+ Mn2+ S2- | B. | Na+ HCO3- Al3+ Cl- | ||
| C. | K+ Na+ Cl- S2- | D. | K+ Cl- Ba2+ OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | SO2通入溴水中 | 溶液褪色 | SO2有漂白性 |
| B | 将Fe(NO3)2样品溶于稀H2SO4,滴加KSCN溶液 | 溶液变红 | Fe(NO3)2样品已氧化变质 |
| C | 向饱和碳酸钠溶液中通入CO2 | 有晶体析出 | 溶解度:NaHCO3>Na2CO3 |
| D | 向盛有少量NaHCO3的试管中滴加草酸溶液 | 有气泡产生 | 酸性:草酸>碳酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 在一定温度下,将冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示.
在一定温度下,将冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
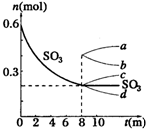 在一个2L的密闭容器中,发生反应2SO3(g)?2SO2(g)+O2(g);△H>0,其中SO3的变化如图所示:
在一个2L的密闭容器中,发生反应2SO3(g)?2SO2(g)+O2(g);△H>0,其中SO3的变化如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 82 | B. | 55 | C. | 137 | D. | 192 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com