
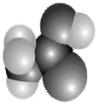
 某常见有机物(只含碳、氢、氧三种元素)分子的比例模型如图所示.请根据其结构特点判断下列有关说法中正确的是( )
某常见有机物(只含碳、氢、氧三种元素)分子的比例模型如图所示.请根据其结构特点判断下列有关说法中正确的是( )| A. | 全部正确 | B. | 只有②错误 | C. | 只有③ | D. | 全部错误 |
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 正极 | Cu | Cu | Zn | Al |
| 负极 | Zn | Zn | Cu | Zn |
| 电解质溶液 | H2SO4 | CuSO4 | ZnCl2 | Cu Cl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 在某有机物A的分子中,具有酚羟基、醇羟基、羧基等官能团,其结构简式如图.
在某有机物A的分子中,具有酚羟基、醇羟基、羧基等官能团,其结构简式如图.

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水银温度计不慎被打破,用胶头滴管将水银吸出放入水封的瓶中,残破的温度计插入装有硫粉在广口瓶中 | |
| B. | 用氢气还原氧化铜的实验中,开始应该先点燃酒精灯后通氢气 | |
| C. | 遇到氯气泄漏时,应立即关闭氯气罐,用浸湿食盐水的毛巾捂住口鼻顺风跑至安全处 | |
| D. | 乘坐火车时,严禁携带白磷、汽油、氯化钠等易燃易爆物品 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
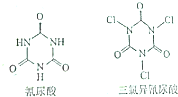 NA表示阿伏加德罗常数的值,下列说法中正确的有几项( )
NA表示阿伏加德罗常数的值,下列说法中正确的有几项( )| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某研究性学习小组,为了探究过氧化钠的强氧化性,设计了如图的实验装置.
某研究性学习小组,为了探究过氧化钠的强氧化性,设计了如图的实验装置.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 《本草纲目》中记载“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”,是用了KNO3的还原性 | |
| B. | 金属钠着火时,可直接用高压水枪喷水扑灭 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,这种提取青蒿素的过程属于化学变化 | |
| D. | 浓H2SO4具有腐蚀性,在其包装上应贴上 的危险警告标签 的危险警告标签 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
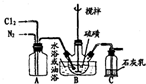 黄红色液体二氯化二硫可以作为贵稀金属的萃取剂,是由硫与氯气在50~60℃直接化合而成.装置图如下:
黄红色液体二氯化二硫可以作为贵稀金属的萃取剂,是由硫与氯气在50~60℃直接化合而成.装置图如下: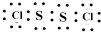 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
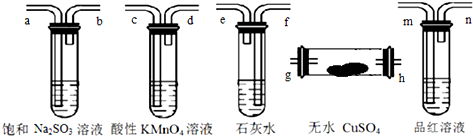
| A. | h-g-m-n-a-b-f-e-c-d | B. | g-h-m-n-a-b-e-f-c-d | ||
| C. | h-g-c-d-m-n-f-e-a-b | D. | h-g-m-n-c-d-e-f-a-b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com