
| A. | 氟化氢 | B. | 水 | C. | 硅化氢 | D. | 二氧化碳 |
分析 在共价化合物中,如果元素化合价的绝对值等于其最外层电子数,则该元素原子最外层电子全部参与成键,据此分析.
解答 解:在共价化合物中,如果元素化合价的绝对值等于其最外层电子数,则该元素原子最外层电子全部参与成键,
A.HF中F元素化合价的绝对值是1,其最外层电子数是7,所以F原子最外层电子不能全部成键,故A错误;
B.H2O中O元素化合价的绝对值是2,其最外层电子数是6,所以O原子最外层电子不能全部成键,故B错误;
C.SiH4中C元素化合价的绝对值是4且其最外层电子数是4,H元素化合价为+1且其最外层电子数是1,所以该反应中Si、H原子最外层电子都全部成键,故C正确;
D.CO2中O元素化合价的绝对值是2,其最外层电子数是6,所以O原子最外层电子不能全部成键,故D错误;
故选C.
点评 本题考查了原子结构,明确原子核外电子排布规律是解本题关键,结合化合物中元素化合价的绝对值与其最外层电子成键的关系来分析解答即可,难度不大.


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ①④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2、CO2、SiO2中的S、C、Si均为sp3杂化 | |
| B. | H3O+、NH4+、[Cu(NH3)4]2+均含有配位键 | |
| C. | SO32-、CO32-、SiO32-均为平面三角形 | |
| D. | 石墨、新型高分子导电材料聚乙炔、金属晶体均含有金属键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:1:2 | B. | 1:2:3 | C. | 3:2:1 | D. | 1:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、MnO4-、K+、NO3- | B. | Na+、Mg2+、SO42-、Cl- | ||
| C. | Na+、Ba2+、OH-、NO3- | D. | K+、SO42-、HCO3-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
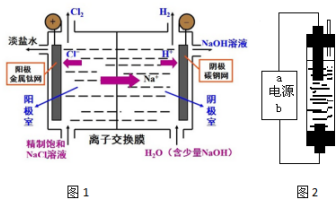
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量的NaOH溶液和盐酸 | B. | 过量的氨水和盐酸 | ||
| C. | 过量的NaOH溶液和二氧化碳 | D. | 过量的氨水和二氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
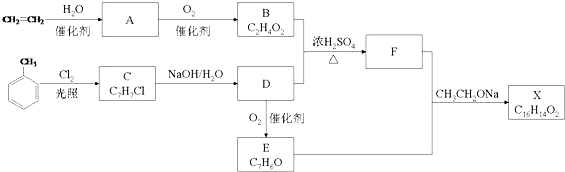

 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O
+2H2O 
 B.
B.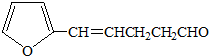
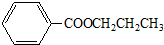
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com