
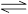 zC���ﵽƽ�⣬����д���пհף�
zC���ﵽƽ�⣬����д���пհף�
 �Ƹ�С״Ԫ�������������ϵ�д�
�Ƹ�С״Ԫ�������������ϵ�д� ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
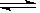 2SO3(g)����Ӧ������ijһʱ��SO2��O2��SO3��Ũ�Ⱦ�Ϊ0.2 mol��L-1�����ﵽƽ��ʱ���ܵ������ǣ� ��
2SO3(g)����Ӧ������ijһʱ��SO2��O2��SO3��Ũ�Ⱦ�Ϊ0.2 mol��L-1�����ﵽƽ��ʱ���ܵ������ǣ� ��| A��c(SO3)="0.4" mol��L-1 | B��c(SO3)= c(SO2)="0.15" mol��L-1 |
| C��c(SO2)="0.25" mol��L-1 | D��c(O2)="0.3" mol��L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
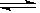 2 SO3 (g); ��H <0, �÷�Ӧ�����Ṥҵ������Ӧ��ȡ�����������ǣ� ��
2 SO3 (g); ��H <0, �÷�Ӧ�����Ṥҵ������Ӧ��ȡ�����������ǣ� ��| A�����¡���ѹ������ | B�����˵��¶ȡ���ѹ������ |
| C�����¡���ѹ������ | D�����˵��¶ȡ���ѹ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
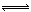 4NO��g����6H2O��g������������ȷ����(���� )��
4NO��g����6H2O��g������������ȷ����(���� )��| A���ﵽƽ��ʱ��4v��(O2)=5v��(NO) |
| B������λʱ��������x mol NO��ͬʱ������x mol NH3,��Ӧ�ﵽƽ��״̬�� |
| C���ﵽƽ��ʱ�������������ݻ���������Ӧ���ʼ�С���淴Ӧ�������� |
| D����ѧ��Ӧ�����ʹ�ϵ�ǣ�2v��(NH3)=3v��(H2O) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 ���������ν��ʹ����е�CO2���������Կ������������˸������ձ����ӡ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״���һ�������·�����Ӧ��CO2(g)��3H2(g)?
���������ν��ʹ����е�CO2���������Կ������������˸������ձ����ӡ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״���һ�������·�����Ӧ��CO2(g)��3H2(g)?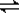 ?CH3OH(g)��H2O(g)����ͼ��ʾ�÷�Ӧ���й���������(��λΪkJ��mol��1)�ı仯��
?CH3OH(g)��H2O(g)����ͼ��ʾ�÷�Ӧ���й���������(��λΪkJ��mol��1)�ı仯��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
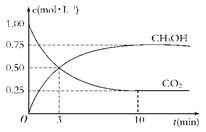
 CO��g����H2��g������ȷ���������淴Ӧ��һ���������Ѵﵽ��ѧƽ��״̬����
CO��g����H2��g������ȷ���������淴Ӧ��һ���������Ѵﵽ��ѧƽ��״̬����| A����ϵ��ѹǿ���ٷ����仯 |
B��v���� CO����v����H2O�� CO����v����H2O�� |
C������n mol CO��ͬʱ ����n mol H2 ����n mol H2 |
| D��1 mol H��H�����ѵ�ͬʱ����2 mol H��O�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 xC��g��,��������ͼ����ʾ��ϵ���ɴ��ƶ϶�ͼ����ȷ˵����
xC��g��,��������ͼ����ʾ��ϵ���ɴ��ƶ϶�ͼ����ȷ˵����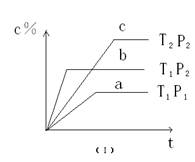
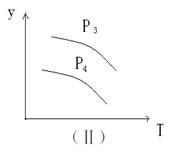
| A��P3��P4 , y���ʾA�İٷֺ��� |
| B��P3��P4 , y���ʾB�İٷֺ��� |
| C��P3��P4 , y���ʾ���������ܶ� |
D��P3��P4 , y���ʾ�������� ƽ����Է������� ƽ����Է������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ���� | X | Y | Z |
| ��ʼŨ��/mol��L-1 | 0.1 | 0.2 | 0 |
| ƽ��Ũ��/mol��L-1 | 0.05 | 0.05 | 0.1 |
 2Z����ƽ�ⳣ��Ϊ1600
2Z����ƽ�ⳣ��Ϊ1600�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 3Z(��)����֪����1 molX��3molY���ﵽƽ�������a mol Z��
3Z(��)����֪����1 molX��3molY���ﵽƽ�������a mol Z�� X��6 mol Y���ﵽƽ���Z�����ʵ���Ϊ ��
X��6 mol Y���ﵽƽ���Z�����ʵ���Ϊ ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com