
| A£® | ÖŠŗĶ10ml 0.1 mol•L-1“×ĖįÓėÖŠŗĶ100ml 0.01 mol•L-1“×ĖįĖłŠčĶ¬ÖÖ¼īČÜŅŗµÄĮæ²»Ķ¬ | |
| B£® | Ģå»żĻąµČ”¢pHĻąµČŃĪĖįŗĶĮņĖįČÜŅŗÖŠ£¬H+Ąė×ÓµÄĪļÖŹµÄĮæĻąµČ | |
| C£® | µČĢå»żpH=3µÄĖįČÜŅŗÓėpH=11µÄ¼īČÜŅŗĻą»ģŗĻŗ󣬻ģŗĻČÜŅŗµÄpHŅ»¶ØµČÓŚ7 | |
| D£® | 250CŹ±£¬½«0.1 mol•L-1NaOHČÜŅŗÓėpH=1µÄĻ”ĮņĖįµČĢå»ż»ģŗĻ£¬»ģŗĻŗóČÜŅŗpH=7 |
·ÖĪö A£®ÖŠŗĶ“×ĖįŠčŅŖĶ¬ÖÖ¼īµÄĪļÖŹµÄĮæÓėĖįµÄĪļÖŹµÄĮæ³ÉÕż±Č£¬ÓėĘäÅØ¶Č“óŠ”ĪŽ¹Ų£»
B£®pHĻąĶ¬Ź±ĖįČÜŅŗÖŠµÄĒāĄė×ÓÅضČĻąµČ£¬µČĢå»żŹ±Į½ČÜŅŗÖŠĒāĄė×ÓµÄĪļÖŹµÄĮæĻąµČ£»
C£®³£ĪĀĻĀ£¬µČĢå»żµÄpH=3µÄĖįČÜŅŗŗĶpH=11µÄ¼īČÜŅŗ»ģŗĻ£¬»ģŗĻŗóČÜŅŗµÄpHæÉÄÜ“óÓŚ7”¢Š”ÓŚ7»ņµČÓŚ7£»
D£®25”ꏱ£¬pH=1µÄĮņĖįÖŠĒāĄė×ÓÅضČĪŖ0.1mol/L£¬ŌņĮ½ČÜŅŗ»ģŗĻŗóĒ”ŗĆ·¢ÉśÖŠŗĶ·“Ó¦£¬ČÜŅŗ³ŹÖŠŠŌ£®
½ā“š ½ā£ŗA£®ÖŠŗĶ“×ĖįŠčŅŖĶ¬ÖÖ¼īµÄĪļÖŹµÄĮæÓėĖįµÄĪļÖŹµÄĮæ³ÉÕż±Č£¬ÓėĘäÅØ¶Č“óŠ”ĪŽ¹Ų£¬Į½ÖÖ“×ĖįµÄĪļÖŹµÄĮæĻąµČ£¬ĖłŅŌĻūŗļīµÄĪļÖŹµÄĮæĻąµČ£¬¹ŹA“ķĪó£»
B£®ŃĪĖį”¢ĮņĖį¶¼ŹĒĒæĖį£¬pHĻąĶ¬Ź±ČÜŅŗÖŠĒāĄė×ÓÅضČĻąµČ£¬ŌņµČĢå»ż”¢µČpHµČµÄŃĪĖįŗĶĮņĖįČÜŅŗÖŠĒāĄė×ÓµÄĪļÖŹµÄĮæĻąµČ£¬¹ŹBÕżČ·£»
C£®³£ĪĀĻĀ£¬µČĢå»żµÄpH=3µÄĖįČÜŅŗŗĶpH=11µÄ¼īČÜŅŗ»ģŗĻ£¬Čē¹ūĖį¼ī¶¼ŹĒĒæµē½āÖŹ£¬Ōņ»ģŗĻČÜŅŗ³ŹÖŠŠŌ£¬Čē¹ūĖįŹĒČõĖį£¬»ģŗĻČÜŅŗ³ŹĖįŠŌ£¬Čē¹ū¼īŹĒČõ¼ī£¬Ōņ»ģŗĻČÜŅŗ³Ź¼īŠŌ£¬ĖłŅŌ»ģŗĻŗóČÜŅŗµÄpHæÉÄÜ“óÓŚ7”¢Š”ÓŚ7»ņµČÓŚ7£¬¹ŹC“ķĪó£»
D£®pH=1µÄĮņĖįČÜŅŗÖŠĒāĄė×ÓÅضČĪŖ0.1mol/L£¬Ōņ½«0.1 mol•L-1NaOHČÜŅŗÓėpH=1µÄĻ”ĮņĖįµČĢå»ż»ģŗĻŗó£¬Į½ČÜŅŗĒ”ŗĆ·“Ó¦£¬ČÜŅŗ³ŹÖŠŠŌ£¬25”ꏱ»ģŗĻŅŗµÄpH=7£¬¹ŹDÕżČ·£»
¹ŹŃ”BD£®
µćĘĄ ±¾Ģāæ¼²éĮĖĖį¼ī»ģŗĻČÜŅŗ¶ØŠŌÅŠ¶Ļ¼°ČÜŅŗpHµÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·ČÜŅŗĖį¼īŠŌÓėČÜŅŗpHµÄ¹ŲĻµĪŖ½ā“š¹Ų¼ü£¬×¢ŅāAÖŠĻūŗļīµÄĪļÖŹµÄĮæÓėĖįµÄÅضČĪŽ¹Ų£¬ĪŖŅדķµć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ī“¼ÓNaOHŹ±£ŗc£ØH+£©£¾c£ØCl-£©=c£ØCH3COOH£© | |
| B£® | ¼ÓČėl0mLNaOHŹ±£ŗc£ØOH-£©+c£ØCH3COO-£©=c£ØH+£© | |
| C£® | ¼ÓČėNaOHÖĮČÜŅŗPh=7Ź±£ŗc£ØClŅ»£©-c£ØNa+£© | |
| D£® | ¼ÓČė20mL NaOHŹ±£ŗc£ØNa+£©=c£ØCl-£©+c£ØCH3COOŅ»'£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚŃõ»Æ»¹Ō·“Ó¦ÖŠ£¬Ńõ»Æ¼ĮÓė»¹Ō¼Į²»Ņ»¶ØŹĒĮ½ÖÖ²»Ķ¬µÄ·“Ó¦Īļ | |
| B£® | ŌŚŃõ»Æ»¹Ō·“Ó¦ÖŠ£¬Éś³ÉĪļ²»Ņ»¶ØŹĒŃõ»Æ²śĪļ»ņ»¹Ō²śĪļ | |
| C£® | ŌŖĖŲÓÉ»ÆŗĻĢ¬×Ŗ»ÆĪŖÓĪĄėĢ¬Ź±£¬øĆŌŖĖŲŅ»¶Ø±»»¹Ō | |
| D£® | ÓŠµ„ÖŹ²Ī¼ÓµÄ·“Ó¦²»Ņ»¶ØŹōÓŚŃõ»Æ»¹Ō·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļ”ĮņĖį | B£® | ŅŅ“¼ | C£® | Ļ”ĻõĖį | D£® | ĒāŃõ»ÆÄĘČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2 4 3 2 2 6 | B£® | 0 2 1 0 1 2 | ||
| C£® | 2 0 1 2 0 2 | D£® | 2 2 2 2 1 4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
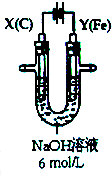 ÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠŹµŃ飮ŹµŃé¹ż³ĢÖŠ£¬Į½¼«¾łÓŠĘųĢå²śÉś£¬Y¼«ĒųČÜŅŗÖš½„±ä³É×ĻŗģÉ«£»Ķ£Ö¹ŹµŃ飬Ģśµē¼«Ć÷ĻŌ±äĻø£¬µē½āŅŗČŌČ»³ĪĒ壮
ÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠŹµŃ飮ŹµŃé¹ż³ĢÖŠ£¬Į½¼«¾łÓŠĘųĢå²śÉś£¬Y¼«ĒųČÜŅŗÖš½„±ä³É×ĻŗģÉ«£»Ķ£Ö¹ŹµŃ飬Ģśµē¼«Ć÷ĻŌ±äĻø£¬µē½āŅŗČŌČ»³ĪĒ壮²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1”¢2 | B£® | 1”¢1 | C£® | 2”¢1 | D£® | 2”¢3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com