
| A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) | B.c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) | D.c(NH4+)>c(Cl-)>c(OH-)>c(H+) |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.95℃纯水的pH<7,说明加热可导致水呈酸性 |
| B.pH=3的醋酸溶液,稀释10倍后pH=4 |
| C.0.2mol/L的盐酸与等体积水混合后pH=1 |
| D.常温下,pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
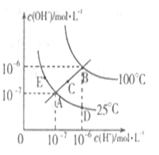
| A.图中五点Kw间的关系:B>C>A=D=E |
| B.若从A点到D点,可采用在水中加入少量酸的方法 |
| C.若从A点到C点,可采用温度不变时在水中加入适量NH4C1固体的方法 |
| D.若处在B点时,将pH =2的硫酸溶液与pH = 10的KOH溶液等体积混合,所得溶液呈中性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.⑦①③②⑨⑤④⑥⑧ | B.⑦①②③⑨④⑤⑥⑧ |
| C.⑧⑥⑤④⑨③②①⑦ | D.①⑦②③⑨④⑥⑤⑧ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.⑤③④②① | B.①②③⑤④ | C.①②③④⑤ | D.⑤③④①② |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在25℃和80℃时纯水中的c[H +] 浓度 |
| B.室温时,浓度均为 0.1 mol·L-1 的 (NH4)2SO4(aq)、(NH4)2CO3 (aq)的 c (NH4+) |
| C.相同条件下,0.l mol·L-1 NaHCO3 和 0.1 mol·L-1 Na2CO3 溶液的 pH |
| D.1 L饱和CH3COONa溶液中CH3COO- 和Na+的个数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=2的CH3COOH与pH=12的NaOH溶液等体积混合 |
| B.0.1 mol/L的CH3COOH溶液与0.2 mol/L的NaOH溶液等体积混合 |
| C.CH3COOH与NaOH溶液混合后所得溶液的pH=7 |
| D.0.1 mol/L的CH3COOH溶液与等物质的量浓度、等体积的NaOH溶液混合 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com