
【题目】下列说法中不正确的是( )
A. 用过滤法除去食盐水中的少量泥沙
B. 用水溶解可除去氢氧化钠中的碳酸钠
C. 用蒸发结晶的方法从食盐水中提取氯化钠
D. 用加热法除去水中溶解的少量氧气
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组采用分类思想、利用抽象方程式:A+H2O→B+C总结相关物质的知识。
(1)若A为单质:
①金属氧化物B常作为磁性材料,则元素A在周期表中的位置为_________。
②A是一种黄绿色气体单质,则生成物中弱电解质的结构式为_________。
③B能腐蚀玻璃,单质C为空气的主要成分之一,写出该反应的化学方程式: _________。
(2)若A为氧化物:
①A为淡黄色固体,则A的电子式为_________。
②A、C均能造成光化学烟雾,则生成1molB转移的电子数目为_________。
(3)若B俗称酒精,C是生活中食用醋的主要成分,则有机物A的名称是_________。另外,A为盐时还可能发生盐类的水解,用以总结水解的规律及微粒浓度的关系等知识。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.10mol/L的盐酸分别滴定20.00mL浓度均为0.10mol/L氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示。

下列说法不正确的是
A. Ⅱ表示的是滴定氨水的曲线,当V(HC1)=20mL时:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B. 当pH=7时,滴定氨水消耗的V(HCl)<20 mL,且c(NH4+)=c(Cl-)
C. 滴定氢氧化钠溶液,V(HCl) >20 mL 时一定有: c(Cl-) >c(Na+) >c(H+) >c(OH-)
D. 当滴定氨水消耗V(HC1)=10 mL 时,有: 2[c(OH-)-c(H+)]=c(NH4+)-c(NH3·H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于氧化还原反应的是( )
A.2NaHCO3 ![]() ?Na2CO3+CO2↑+H2O
?Na2CO3+CO2↑+H2O
B.H2SO4+CuO═CuSO4+H2O
C.2 H2S+SO2═3S↓+2H2O
D.CO2+Ca(OH)2═CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍具有铁磁性和延展性,能导电和导热。镍单质及其化合物的化学性质与铁相似。
(1)镍易溶于稀的无机酸中,并放出氢气,写出镍与盐酸反应的化学方程式:_____________。
(2)在隔绝空气的条件下,加热NiC2O4使其分解,就能得到暗绿色的氧化亚镍,写出该反应的化学方程式: _____________。
(3)Ni2O3不溶于水,可溶于盐酸并放出氯气,写出该反应的离子方程式: _____________。
(4)氢镍电池是一种碱性可充电电池,污染小,比能量较大。氢镍电池的总反应式是:H2+2NiO(OH) ![]() 2Ni(OH)2。写出放电时的正极反应式: _____________。
2Ni(OH)2。写出放电时的正极反应式: _____________。
(5)纳米材料镍粉(Ni)是一种高性能电极材料,其制备过程如下:
步骤I:取0.2mol/L的硝酸亚镍溶液,调节pH除铁后,加入活性炭过滤。
步骤Ⅱ:向所得滤液中滴加1.5mol/L的NaHCO3溶液使Ni2+完全沉淀,生成:xNiCO3·yNi(OH)2·zH2O。
步骤Ⅲ:将产生的沉淀用大量高纯水清洗并用离心机甩干。
步骤Ⅳ:加入稍过量的肼溶液(N2H4·H2O),使上述沉淀还原完全,将生成的Ni水洗后,再用95%的乙醇浸泡后晾干。为测定xNiCO3·yNi(OH)2·zH2O的组成,进行如下实验:
①准确称取7.54g样品与过量的肼溶液(N2H4·H2O)充分反应,共收集到1.12LN2和CO2的混合气体(已换算成标准状况)。
②另取等质量的样品充分灼烧,冷却后称得残留固体NiO的质量为4.5g。
通过计算确定xNiCO3·yNi(OH)2·zH2O的化学式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某学生拟用图1所示装置模拟工业制取并收集ClO2。
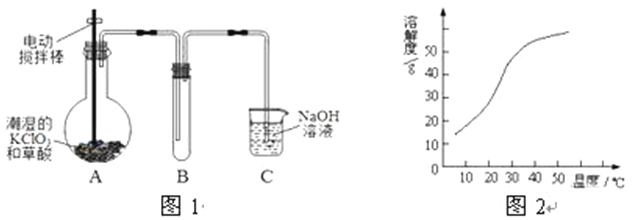
(1) A 装胃电动搅抖柞的作用是___________
(2)B装置必须放在冰水浴中,其原因是___________
(3)反应后在装置C中可得NaClO2溶液。已知I.NaClO2饱和溶液在温度低了38℃时析出晶体是NaClO2·3H2O,在温度高于38℃时析出晶体是NaClO2, 温度高于60℃时NaClO2分解生成NaClO3和NaCl;
Ⅱ.NaClO2的溶解度曲线如图2所示,请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:
①减压,55℃蒸发结晶;②__________;③用38℃~60℃热水洗涤;④_____;得到成品。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样;量取V1mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用cmol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL(已知2 Na2S2O3+ I2=Na2S4O6+ 2NaI)。
①配制100 mLcmol·L-1Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有:____________。
②原ClO2溶液的浓度为_________g/L(用含字母代数式表示)。
③若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果____________。(填“偏高”、“偏低”或“不变” )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在制玻璃的原料中,再加入下列物质后,可制得各种不同用途的玻璃:
a.氧化亚铜(Cu2O) b.氧化钴(Co2O3)
c.氧化铅(PbO) d.硼砂(Na2B4O7·10H2O)
①制造化学仪器的玻璃需加入的物质是。
②制造光学仪器的玻璃需加入的物质是。
③制造蓝色玻璃需加入的物质是。
④制造红色玻璃需加入的物质是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关海水综合利用的说法正确的是
A. 海水中含有钾元素,只需经过物理变化就可以得到钾单质
B. 海水蒸发制海盐的过程中只发生了化学变化
C. 从海水中可以得到NaCl,电解熔融NaCl可制备Na和Cl2
D. 利用潮汐发电是将化学能转化为电能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com