
| A. | 原子半径:W>Z>Y>X | B. | 气态氢化物的稳定性:X<Z | ||
| C. | 最外层电子数:Y>W | D. | Y、z的氧化物都是两性氧化物 |
分析 X、Y、Z、W为周期表中前20号元素中的四种,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故X为O元素;Z单质是一种良好的半导体,则Z为Si;W、Y为金属元素,W原子序数大于Si,故W处于第四周期,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等,由于X处于IIA族,Y原子最外层电子数为4,Y、Z不可能同周期,则X处于IA族,Y处于ⅢA族,可推知W为K、Y为Al,据此解答.
解答 解:X、Y、Z、W为周期表中前20号元素中的四种,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故X为O元素;Z单质是一种良好的半导体,则Z为Si;W、Y为金属元素,W原子序数大于Si,故W处于第四周期,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等,由于X处于IIA族,Y原子最外层电子数为4,Y、Z不可能同周期,则X处于IA族,Y处于ⅢA族,可推知W为K、Y为Al.
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:K>Al>Si>O,故A错误;
B.非金属性O>Si,氢化物稳定性与元素非金属性一致,故氧元素氢化物较稳定,故B错误;
C.Y为Al,原子最外层电子数为3,W为K,原子最外层电子数为1,故最外层电子数:Y>W,故C正确;
D.Y、Z的氧化物分别为氧化铝、二氧化硅,氧化铝是两性氧化物,二氧化硅属于酸性氧化物,故D错误,
故选:C.
点评 本题考查结构性质位置关系综合应用,推断元素是解题关键,侧重考查学生的分析推理能力及元素周期律.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 该氨水显弱碱性 | |
| B. | 加水稀释过程中,c(H+)/c(OH-)的值减小 | |
| C. | 与同温下pH=11的NaOH溶液相比,NaOH溶液中c(Na+)大于氨水中c(NH4+) | |
| D. | 加入少量NH4Cl 固体,溶液中水的电离平衡:H2O?H++OH-向右移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 常温时向浓度为0.1mol/L体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应.根据图象回答下列问题:
常温时向浓度为0.1mol/L体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应.根据图象回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.05 mol•L-1H2CrO4溶液的pH=1 | |
| B. | 向100 mL0.l mol•L-1 H2CrO4溶液中滴入几滴NaOH溶液,溶液中$\frac{c(Cr{O}_{4}^{2-})}{c(HCr{O}_{4}^{-})}$变大 | |
| C. | Na2CrO4溶液中:c(Na+)+c(H+)=c(CrO42-)+c(HCrO4-)+c(OH-) | |
| D. | 等浓度的:NaHCrO4溶液与NaHCO3溶液中,水的电离程度前者大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
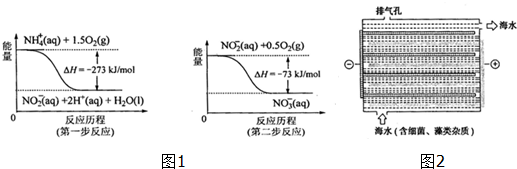
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度(mol/L) | 3×10-6 | 7×10-6 | 2×10-5 | 3×10-5 | 5×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.1mol•L-1CH3COOH与0.1mol•L-1氨水等体积混合(PH=7):c(NH4+)=c(CH3COO-)=c(H+)=c(OH-) | |
| B. | 0.1mol•L-1HCl溶液与0.2mol•L-1氨水等体积混合(PH>7):c(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-) | |
| C. | 0.1mol•L-1CH3COONa与0.1mol•L-1CaCl2溶液等体积混合:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) | |
| D. | 0.1mol•L-1Na2CO3溶液与0.1mol•L-1 NaHCO3溶液等体积混合:c(HCO3-)>0.05mol•L-1>c(CO32-)>c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com