
拆开1 mol 共价键所吸收的能量或形成1 mol 共价键所释放的能量称为键能。已知:H-H键能为436 kJ /mol,H-N键能为391 kJ /mol, N2 (g)+ 3H2(g) 2NH3(g) ΔH=-92.4 kJ /mol,下列说法中正确的是
2NH3(g) ΔH=-92.4 kJ /mol,下列说法中正确的是
| A.H-H比N≡N更牢固 |
| B.N≡N键能约为946 kJ/mol |
| C.合成氨反应选择适当的催化剂是为了提高H2的转化率 |
| D.0.5 mol N2和1.5 mol H2在题给条件下充分反应,放出热量为46.2 kJ |
B
解析试题分析:反应热等于生成物中断键吸收的热量和形成反应物中化学键放出的热量之差,则如果假设N≡N键能为x,则根据热化学方程式可知x+3×436 kJ/mol-2×3×391 kJ/mol=-92.4 kJ/mol,解得x=946 kJ/mol,所以B正确;A、H-H比N≡N键能小,所以N≡N比H-H更牢固,A不正确;C、催化剂只能改变反应速率,而不能改变平衡状态,所以合成氨反应选择适当的催化剂不是为了提高H2的转化率,C不正确;D、由于该反应是可逆反应,因此0.5 mol N2和1.5 mol H2在题给条件下充分反应,放出热量小于46.2 kJ,D不正确,答案选B。
考点:考查反应热的计算、应用以及催化剂对反应速率和平衡状态的影响


 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源: 题型:单选题
信息、材料、能源被称为新科技革命的“三大支柱”。下列观点或做法错误的是
| A.在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源 |
| B.加大煤炭的开采速度,增加煤炭燃料的供应量,以缓解石油危机 |
| C.光缆在信息产业中有广泛应用,制造光缆的主要材料是二氧化硅 |
| D.高温结构陶瓷氮化硅(Si3N4)具有较高的硬度和耐磨性,可用于制造汽车发动机 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据下列热化学方程式:
(1)C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1
(2)H2(g)+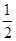 O2(g)=H2O(l) ΔH2=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH2=-285.8 kJ·mol-1
(3)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH3=-870.3 kJ·mol-1
可以计算出2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热为 ( )
| A.ΔH=+244.1 kJ·mol-1 |
| B.ΔH=-488.3 kJ·mol-1 |
| C.ΔH=-996.6 kJ·mol-1 |
| D.ΔH=+996.6 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
工业生产水煤气的反应为:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.4 kJ/mol,下列判断正确的是( )
| A.反应物能量总和小于生成物能量总和 |
| B.CO(g)+H2(g)=C(s)+H2O(g) ΔH=+131.4 kJ/mol |
| C.水煤气反应中,生成1 mol H2(g)吸收131.4 kJ热量 |
| D.水煤气反应中生成1体积CO(g)吸收131.4 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述正确的是 ( )
| A.推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应 |
| B.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” |
| C.用电解水的方法制取大量氢气可以缓解能源不足的问题 |
| D.升高温度活化能降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示:
① H2(g)+I2(?) 2HI(g)+9.48kJ② H2(g)+I2(?)
2HI(g)+9.48kJ② H2(g)+I2(?) 2HI(g)-26.48kJ
2HI(g)-26.48kJ
下列判断正确的是
| A.①中的I2为固态,②中的I2为气态 |
| B.②的反应物总能量比①的反应物总能量低 |
| C.①的产物比反应②的产物热稳定性更好 |
| D.1mol 固态碘升华时将吸热17kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O(1) △H=-57.3kJ/mol。向1L0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时的热效应△H1、△H2、△H3的关系正确的是
| A.△H1>△H2>△H3 | B.△H1<△H3<△H2 | C.△H1<△H2<△H3 | D.△H1>△H3>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列热化学方程式正确的是(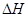 的绝对值均正确)
的绝对值均正确)
| A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H=-1367.0 kJ/mol(燃烧热) |
| B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热) |
| C.S(s)+O2(g)=SO2(g)△H=-269.8kJ/mol(反应热) |
| D.2NO2=O2+2NO△H= +116.2kJ/mol(反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图所示是101kPa时,氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )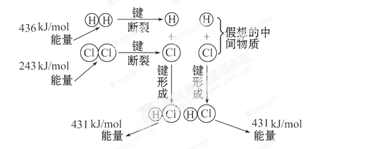
| A.此反应的热化学方程式为:H2(g)+Cl2(g) =2HCl(g) ΔH=+183kJ·mol-1 |
| B.2molHCl分子中的化学键形成时要释放862kJ能量 |
| C.1molH2中的化学键断裂时需要吸收436kJ能量 |
| D.此反应的热化学方程式为:1/2H2(g)+1/2Cl2(g) =HCl(g) ΔH=-91.5kJ·mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com