
【题目】19世纪中叶,门捷列夫总结了如表所示的元素化学性质的变化情况。请回答:

(1)门捷列夫的突出贡献是________。
A.提出了原子学说
B.提出了分子学说
C.发现了元素周期律
D.发现能量守恒定律
(2)该表变化表明________。
A.事物的性质总是在不断地发生变化
B.元素周期表中最右上角的氦元素是非金属性最强的元素
C.第ⅠA族元素的金属性肯定比同周期的第ⅡA族元素的金属性强
D.物质发生量变到一定程度必然引起质变
(3)按照表中元素的位置,认真观察从第ⅢA族的硼到第ⅦA族的砹连接的一条折线,我们能从分界线附近找到________。
A.耐高温材料 B.新型农药材料
C.半导体材料 D.新型催化剂材料
(4)据报道,美国科学家制得一种新原子![]() X,它属于一种新元素116号元素(元素符号暂用X代替),关于它的推测正确的是________。
X,它属于一种新元素116号元素(元素符号暂用X代替),关于它的推测正确的是________。
A.这种原子的中子数为167
B.它位于元素周期表中第6周期
C.这种元素一定是金属元素
D.这种元素的原子易与氢化合
【答案】 C )CD C AC
【解析】(1)A.19世纪初,英国化学家道尔顿提出近代原子学说,A错误;B.19世纪初,意大利科学家阿伏加德罗提出分子概念,提出原子-分子学说,B错误;C.1869年,俄国化学家门捷列夫发现了元素周期律,并编制出元素周期表,使得化学学习和研究变得有规律可循,C正确;D.1756年俄国罗蒙诺索夫首先能量守恒定律,D错误;答案选C。(2)A.图示显示不同元素的递变规律,A错误;B.氦为稀有气体,性质最稳当,B错误;C.同周期,从左到右,金属性减弱,ⅠA族元素的失电子能力肯定比同周期ⅡA族元素的失电子能力强,C正确;D.同周期,随原子序数递增,元素从活泼金属→金属→两性元素→非金属→活泼非金属排列,物质发生量变到一定程度必然引起质变,D正确;答案选CD;(3)耐高温的合金材料在过渡元素区寻找;制农药的元素在周期表右上方的非金属元素区寻找;做催化剂的元素从过渡元素区寻找;作半导体材料的元素,在元素周期表金属元素与非金属元素的分界线附近寻找,而从ⅢA族的硼到ⅦA族的砹是元素周期表金属元素与非金属元素的分界线,所以作半导体材料的元素,答案选C;(4)稀有气体的原子序数分别为:2、10、18、36、54、86、118,116号元素与118号元素同周期,且位于118号元素的前2列,即116号元素处于第七周期ⅥA族,A.质量数为283,质子数为116,所以中子数为167,A正确;B.116号元素处于第七周期ⅥA族,B错误;C.该元素的金属性比Po强,一定为金属元素,C正确;D.该元素为金属元素,金属性比较弱,不易与氢化合,D错误,答案选AC。


科目:高中化学 来源: 题型:
【题目】铟产业被称为“信息时代的朝阳产业”.元素周期表中铟的数据如图,下列说法完全正确的是( ) 
A.铟元素的质量数是114.8
B.铟元素的相对原子质量是114
C.铟元素是一种副族元素
D.铟原子最外层有3个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y 各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表,下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率v(Z)=2.0×10﹣3 mol/(Lmin)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的溶液,造成浓度偏高的操作是
A.定容时,滴加蒸馏水超过刻度线
B.定容时,眼睛俯视刻度线
C.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
D.定容时,眼睛仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为倡导“低碳”,减小CO2对环境的影响,需对CO2进行创新利用研究.T1℃使,将将9mol CO2和12mol H2充入3L密闭容器中,发生反应CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H<0,容器中CH3OH的物质的量随时间变化如曲线Ⅰ所示,平衡时容器内压强为p0 . 改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线Ⅱ所示.下列说法错误的是( ) 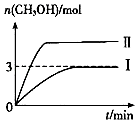
A.曲线Ⅱ对应的条件改变是增大压强
B.T2℃时,上述反应平衡常数为0.52,则T2>T1
C.在T1℃,若起始时向容器充入4.5 mol CO2、6 mol H2 , 平衡时容器内压强P1> ![]()
D.在T1℃,若起始时向容器中充入4.5 mol CO2、5 mol H2、5 mol CH3OH(g)和5 mol H2O(g),则达平衡前v(正)>v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某次实验需用0.4molL﹣1 NaOH溶液480mL.配制方法如下:
(1)用托盘天平准确称量g 固体NaOH;
(2)将称量好的NaOH固体放在500mL大烧杯中,倒入约300mL蒸馏水,用玻璃棒搅拌,使固体全部溶解,待后,将烧杯中的溶液注入容量瓶中;
(3)用少量蒸馏水洗涤烧杯次,洗涤后的溶液 , 轻轻晃动容量瓶,使溶液混合均匀;
(4)向容量瓶中加入蒸馏水,到液面时,改用加蒸馏水至液面最低点与刻度线相切.盖好瓶塞,;
(5)若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏高的是 , 偏低的是 , 对实验结果没有影响的是(填各选项的序号). A.所用的NaOH中混有少量Na2O
B.用托盘天平称量一定质量固体NaOH时,所用的小烧杯内壁不太干燥
C.配制溶液所用的容量瓶洗净后没有烘干
D.固体NaOH在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作
E.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
F.最后确定NaOH溶液体积(定容)时,俯视观察液面与容量瓶刻度线
G.定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com