
【题目】下表为八种短周期主族元素的部分性质(已知铍的原子半径为0.89×10-10m):
元素代号 | X | Y | Z | M | R | J | Q | T |
原子半径/10-10m | 0.74 | 0.75 | 0.99 | 1.86 | 1.43 | 1.10 | ||
主要化合价 | -2 | +5、-3 | +4、-4 | +7、-1 | +1 | +3 | +5、-3 | |
其它 | 原子核内无中子 | 无机非金属材料主角 | 有两种氧化物 |
(1)元素M在元素周期表中的位置为_________________________。
(2)写出X、Y、J三种元素形成的化合物电子式_________。用电子式表示X元素与Z元素形成化合物的过程:_______________________。
(3)写出Y与Q两种元素形成的化合物与J的最高价氧化物的水化物反应的离子方程式_____。
(4)R与T相比,非金属性较强的是____(用元素符号表示),下列事实能证明这一结论的是_______(填字母)。
A.常温下T的单质呈固态,R的单质呈气态
B.R的氢化物比T的氢化物稳定
C.R的氢化物水溶液酸性比T的氧化物对应水化物酸性强
D.R与T形成的化合物中T呈正价
(5)J与Q相比,金属性较强的是____(用元素符号表示),能证明这一结论的依据是______。
(6)根据表中数据推测,M的原子半径的最小范围是 ____________________。
【答案】 第三周期 IVA族 ![]()
![]() Al2O3+ 2OH— = 2AlO2—+ H2O Cl BD Na Na能与冷水反应,Al与冷水不反应[或NaOH的碱性比Al(OH)3强等] 大于1.10×10-10m,小于1.43×10-10 m
Al2O3+ 2OH— = 2AlO2—+ H2O Cl BD Na Na能与冷水反应,Al与冷水不反应[或NaOH的碱性比Al(OH)3强等] 大于1.10×10-10m,小于1.43×10-10 m
【解析】X原子核内无中子,X为H,Z和T主要化合价+5、-3,为ⅤA族元素,Z原子半径小,为N元素,T为P,Y主要化合价为-2,半径比N小,故Y为O元素,M无机非金属材料主角,M为硅,R主要化合价+7、-1,R为氯元素,J有两种氧化物,+1价,故J为钠元素,Q主要化合价+3价,为铝元素。(1)元素M为硅,在元素周期表中的位置为第三周期 、IVA族。(2)X、Y、J三种元素形成的化合物氢氧化钠,电子式![]() 。N与H通过共用电子对形成NH3,用电子式表示X元素与Z元素形成化合物的过程:
。N与H通过共用电子对形成NH3,用电子式表示X元素与Z元素形成化合物的过程:![]() 。(3)Y与Q两种元素形成的化合物Al2O3与J的最高价氧化物的水化物NaOH反应的离子方程式Al2O3+ 2OH— = 2AlO2—+ H2O 。(4)同一周期从左到右非金属性增强,P与Cl相比,非金属性较强的是Cl(用元素符号表示);下列事实能证明这一结论的是BD(填字母)。A.非金属性与元素的状态没有必然的联系,故A错误;B.R的氢化物比T的氢化物稳定强,非金属性强,故B正确;C.要比较最高价氧化物对应水化物酸性强弱,故C错误;D.R与T形成的化合物中T呈正价,非金属性强的的元素显负价,故D正确;故选BD。(5)J与Q相比,金属性较强的是Na (用元素符号表示),能证明这一结论的依据是 Na能与冷水反应,Al与冷水不反应[或NaOH的碱性比Al(OH)3强等]。(6)根据表中数据推测,同周期从左到右原子半径变小,M的原子半径的最小范围是:大于P原子1.10×10-10m,小于铝原子1.43×10-10 m。
。(3)Y与Q两种元素形成的化合物Al2O3与J的最高价氧化物的水化物NaOH反应的离子方程式Al2O3+ 2OH— = 2AlO2—+ H2O 。(4)同一周期从左到右非金属性增强,P与Cl相比,非金属性较强的是Cl(用元素符号表示);下列事实能证明这一结论的是BD(填字母)。A.非金属性与元素的状态没有必然的联系,故A错误;B.R的氢化物比T的氢化物稳定强,非金属性强,故B正确;C.要比较最高价氧化物对应水化物酸性强弱,故C错误;D.R与T形成的化合物中T呈正价,非金属性强的的元素显负价,故D正确;故选BD。(5)J与Q相比,金属性较强的是Na (用元素符号表示),能证明这一结论的依据是 Na能与冷水反应,Al与冷水不反应[或NaOH的碱性比Al(OH)3强等]。(6)根据表中数据推测,同周期从左到右原子半径变小,M的原子半径的最小范围是:大于P原子1.10×10-10m,小于铝原子1.43×10-10 m。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】铜、镁合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只产生4480mL 的NO2气体和336mL的N2O4气体(均为标准状况下),在反应后的溶液中加入足量的NaOH溶液,生成的沉淀的质量为( )
A.7.04g
B.8.26g
C.8.51g
D.9.02g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00 mL 0.1000 mol·L—1 (NH4)2SO4溶液中逐滴加入0.2000 mol·L—1NaOH时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。下列说法正确的是

A.点a所示溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-)
B.点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-)
C.点c所示溶液中:c(SO42-)+ c(H+)= c(NH3·H2O )+ c(OH-)
D.点d所示溶液中:c(SO42-)>c(NH3·H2O )>c(OH-)>c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G都是有机化合物,它们的转化关系如下: 
请回答下列问题:
(1)已知:6.0g化合物E完全燃烧生成8.8g CO2和3.6g H2O;E的蒸气对氢气的相对密度为30,则E的分子式为 .
(2)A为一取代芳烃,B中含有一个甲基.由B生成C的化学方程式为 .
(3)由B生成D、由C生成D的反应条件分别是、 .
(4)由A生成B、由D生成G的反应类型分别是、 .
(5)F存在于栀子香油中,其结构简式为 .
(6)在G的同分异构体中,苯环上一硝化的产物只有一种的共有种,其中核磁共振氢谱有两组峰,且峰面积比为l:1的是(填结构简式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A. 标准状况下,2.24 L![]() 中含有碳碳双键数为0.3NA
中含有碳碳双键数为0.3NA
B. 0.1mol甲烷和乙烯组成的混合气体完全燃烧,生成的水分子数为0.2NA
C. 0.1molCH4与0.1molCl2混合充分光照,生成CH3Cl分子数为0.1 NA
D. 0.1molN2和0.3molH2在高温、高压及催化剂下充分反应,产物的分子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硅酸的反应为Na2SiO3+2HCl═2NaCl+H2SiO3↓,该反应属于( )
A.化合反应
B.分解反应
C.置换反应
D.复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述一定正确的是
A. 2.0gH218O和D2O的混合物中含有质子数为NA
B. 1.0L2.0mol/LNaOH溶液中含有氧原子数为2NA
C. 3.4gH2O2参加氧化还原反应时转移电子数为0.1 NA
D. 标准状况下2.24L的CCl4含有共价键数目为0.4 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种短周期元素在周期表中的位置如图,X通过共用三对电子形成X2分子,下列说法不正确的是
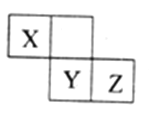
A. 化合物XZ3中各原子均满足8电子的稳定结构
B. X、Y、Z三种元素形成的含氧酸都是强酸
C. 常温下,Z单质可与Y的氢化物发生置换反应
D. 一定条件下,X2与Al反应得到AlX
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案鉴别Na2CO3和NaHCO3两种白色粉末,不能达到预期目的的是( )
A. 分别向等量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢
B. 分别向等量的白色粉末中加等体积适量的水,比较固体溶解量的多少
C. 分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成
D. 分别将等量的白色粉末用如图装置进行实验,比较澄清石灰水是否变浑浊
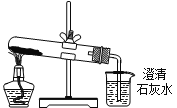
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com