
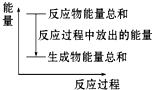
| A. | 反应过程中能量关系可用如图表示: | |
| B. | 若将该反应设计成原电池,锌为负极 | |
| C. | 若将该反应设计成原电池,正极可用石墨 | |
| D. | 若将其设计为原电池,当有32.5 g锌溶解时,正极放出的气体一定为11.2 L |
分析 对于Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g),反应为放热反应,则反应物的总能量大于生成物的总能量,当将该反应设计呈原电池时,Zn为负极,被氧化,正极为不如锌活泼的金属或者石墨上析出氢气,以此解答该题.
解答 解:A.反应为放热反应,则反应物的总能量大于生成物的总能量,图示正确,故A正确;
B.反应中Zn被氧化生成ZnSO4,当将该反应设计呈原电池时,Zn为负极,故B正确;
C.反应中Zn被氧化生成ZnSO4,当将该反应设计呈原电池时,Zn为负极,正极为不如锌活泼的金属或者石墨,故C正确;
D.若将其设计为原电池,当有32.5g锌溶解时,转移电子1mol,则正极放出气体的体积在标况下为11.2L,未指明标况下就不一定为11.2 L,故D错误.
故选D.
点评 本题考查化学反应能量的变化,题目难度不大,本题注意反应热以及原电池的工作原理,学习中注意相关知识的理解和掌握.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
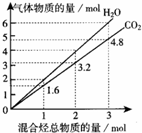 两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法错误的是( )
两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法错误的是( )| A. | 该混合气体中一定含有乙烯 | |
| B. | 该混合气体中有且只有一种烷烃 | |
| C. | 组成该混合气体的烃分子所含氢原子数均为4 | |
| D. | 若混合气体由CH4和C2H4组成,则其体积比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷与Cl2反应制氯乙烷 | B. | 乙醇和浓硫酸共热制乙烯 | ||
| C. | 乙酸和乙醇共热酯化 | D. | 乙烯与氧气在银催化作用下生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能得到一种醛 | B. | 能得到二种醛 | ||
| C. | 能得到三种醛 | D. | 该反应为取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
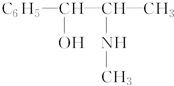
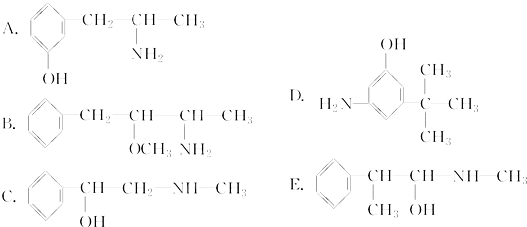
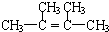 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③④ | C. | ④ | D. | ①②⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 时间/s | 5 | 10 | 15 | 20 | 25 |
| n(CO2)/mol | 0.04 | 0.06 | 0.07 | 0.08 | 0.08 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com