
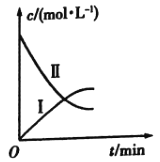
【题目】某实验探究小组研究320K时![]() 的分解反应:
的分解反应:![]() 。如图是该小组根据所给表格中的实验数据绘制的。下列有关说法正确的是( )
。如图是该小组根据所给表格中的实验数据绘制的。下列有关说法正确的是( )
t/min | 0 | 1 | 2 | 3 | 4 |
| 0.160 | 0.114 | 0.080 | 0.056 | 0.040 |
| 0 | 0.023 | 0.040 | 0.052 | 0.060 |
A.曲线Ⅰ是![]() 的浓度变化曲线
的浓度变化曲线
B.曲线Ⅱ是![]() 的浓度变化曲线
的浓度变化曲线
C.![]() 的浓度越大,反应速率越快
的浓度越大,反应速率越快
D.![]() 的浓度越大,反应速率越快
的浓度越大,反应速率越快
科目:高中化学 来源: 题型:
【题目】在密闭容器,一定条件下进行反应:mA(g)+nB(g)pC(g)+qD(g)。若增大压强或升高温度,重新达到平衡,变化过程均如图所示,则对该反应叙述正确的是( )
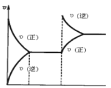
A.m+n<p+qB.逆反应是放热反应
C.m+n>p+qD.正反应是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中的下列做法不合理的是( )
①实验室中钠着火时,用泡沫灭火器灭火
②实验室保存氯化亚铁溶液时加入适量铁粉
③用饱和碳酸钠溶液除去二氧化碳气体中的氯化氢
④用水除去一氧化氮气体中的二氧化氮
⑤用浓硫酸干燥硫化氢气体
⑥用氢氧化钠溶液除去氧化铁中的氧化铝
A.①②③B.③④⑤C.①③⑤D.②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,对应的操作、现象以及所得出的结论都正确的是( )
选项 | 实验 | 现象 | 结论 |
A. | 把铝箔插入浓硝酸中 | 有大量红棕色气体产生 | 浓硝酸具有强氧化性 |
B. |
| 品红褪色 |
|
C. | 淀粉在酸催化水解后的溶液加入新制 | 无砖红色沉淀 | 淀粉水解产物不含葡萄糖 |
D. | 将充满 | 红棕色变深 | 反应 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据图示填空。
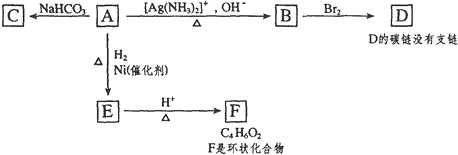
(1)化合物A含有的官能团是___________________________________。
(2)1mol A与2mo H2反应生成1moE,其反应方程式是________________。
(3)与A具有相同官能团的A的同分异构体的结构简式是_____________。
(4)B在酸性条件下与Br2反应得到D,D的结构简式是________________。
(5)F的结构简式是___________。由E生成F的反应类型是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃在化工生产过程中有重要意义。如图所示是以烯烃A为原料合成粘合剂M的路线图。
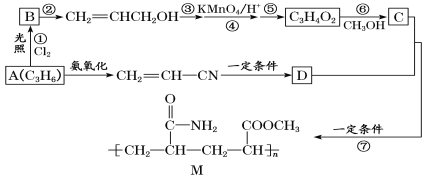
回答下列问题:
(1)下列关于路线图中的有机物或转化关系的说法正确的是__(填字母)。
a.A能发生加成反应、氧化反应、缩聚反应
b.B的结构简式为CH2ClCHClCH3
c.C的分子式为C4H5O3
d.M的单体是CH2=CHCOOCH3和![]()
(2)A分子中所含官能团的结构简式是__反应①的反应类型为__。
(3)设计反应③⑤的目的是__,C的名称为__。
(4)C和D生成M的化学方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下将0.01molNH4Cl和0.002molNaOH溶于水配成1L溶液。
①该溶液中除H2O的电离平衡外还存在的平衡体系是___。
②溶液中共有___种不同的微粒。
③这些粒子中浓度为0.01mol·L-1的是___,浓度为0.002mol·L-1的是___。
④物质的量之和为0.01mol的两种微粒是___。
(2)某二元酸(化学式用H2B表示)在水中的电离方程式是H2B=H++HB-;HB-![]() H++B2-,回答下列问题:
H++B2-,回答下列问题:
①已知0.1mol·L-1NaHB溶液的pH=2,则0.1mol·L-1H2B溶液中c(H+)___(填“<”、“>”、“=”)0.11mol·L-1理由是___。
②0.1mol·L-1NaHB溶液中各种离子浓度由大到小的顺序是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用氯化铁浸出一重铬酸钾(K2Cr2O7)滴定法测定钛精粉试样中单质铁的质量分数[ω(Fe)%],实验步骤如下:
步骤1:称取试样0.100g于250mL洗净的锥形瓶中。
步骤2:加入FeCl3溶液100mL,迅速塞上胶塞,用电磁搅拌器搅拌30min。
步骤3:过滤,用水洗涤锥形瓶和滤渣各3~4次,洗液全部并入滤液中。
步骤4:将滤液稀释至500mL,再移取100mL稀释液于锥形瓶中,加入20mL硫酸和磷酸的混合酸,加0.5%二苯胺磺酸钠指示剂4滴。
步骤5:以K2Cr2O7标准溶液滴定至出现明显紫色为终点。发生的反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
步骤6:重复测定两次,数据如下:
第一次 | 第二次 | 第三次 | |
消耗的K2Cr2O7标准溶液体积(mL) | 10.01 | 9.99 | 13.00 |
步骤7:数据处理。
(1)步骤2中加入FeCl3溶液后锥形瓶中发生反应的离子方程式为___,迅速塞上胶塞的原因是___。
(2)步骤3中判断滤纸上残渣已洗净的方法是___。
(3)实验中需用到100mL浓度约为0.01mol·L-1K2Cr2O7标准溶液,配制时用到的玻璃仪器有___;称量K2Cr2O7固体前应先将其烘干至恒重,若未烘干,对测定结果的影响是___(填“偏高”、“偏低”或“无影响”);滴定时,K2Cr2O7溶液应置于___(填仪器名称)中。
(4)利用上表数据,计算出该钛精粉试样中单质铁的质量分数为___(写出必要的计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应与能量的说法正确的是( )
A.Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s) ΔH=-216kJ·mol-1,E反应物<E生成物
B.CaCO3(s)=CaO(s)+CO2(g) ΔH=+178.2kJ·mol-1,E反应物<E生成物
C.2HCl(g)=H2(g)+Cl2(s) ΔH=+92.3kJmol-1,1molHCl在密闭容器中分解后放出92.3kJ的能量
D.将0.5molN2和1.5molH2置于密闭的容器中充分反应后生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6kJ·mol-1
2NH3(g) ΔH=-38.6kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com