
| A. | CH3C≡CCH3 | B. | CH2=CH2 | C. | CH≡CCH3 | D. | CH2=CHCH3 |
分析 某气态烃1mol能与2mol HCl完全加成,说明该烃中含有一个碳碳三键或2个碳碳双键,加成后产物分子上的氢原子又可被6mol Cl2完全取代,说明加成后的物质含有6个H原子,据此确定该烃.
解答 解:某气态烃1mol能与2mol HCl完全加成,说明该烃中含有一个碳碳三键或2个碳碳双键,加成后产物分子上的氢原子又可被6mol Cl2完全取代,说明加成后的物质含有6个H原子,加成后的烃比加成前的烃多2个H原子,所以加成前的烃含有4个H原子,丙炔中含有一个碳碳三键且含有4个H原子,则丙炔符合条件,
故选C.
点评 本题以物质的推断为载体考查了取代反应和加成反应,明确反应时分子中的变化是解本题的关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M | B. | M+ | C. | M2+ | D. | M3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
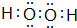 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酸性KMnO4溶液鉴别乙烯和乙炔 | |
| B. | 检验C2H5Cl中氯原子时,将C2H5Cl和NaOH溶液混合加热后,加入稀硫酸进行酸化 | |
| C. | 酒精与稀硫酸加热到170℃制乙烯 | |
| D. | 制取溴苯应用液溴、铁屑和苯混合,反应后并用稀碱液洗涤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com