
分析 (1)固体的质量增加了2.80g为Si3N4的质量,根据n=$\frac{m}{M}$计算其物质的量,根据方程式计算消耗氢气的物质的量,再根据v=$\frac{\frac{△n}{V}}{△t}$计算v(H2);
平衡常数为生成物浓度化学计量数次数幂之积与生成物浓度化学计量数次数幂之积的比值;
(2)a.平衡常数只受温度影响;
b.正反应为放热反应,升高温度平衡向逆反应方向移动,平衡常数减小;
c.Si3N4是固体,增大其物质的量,不影响平衡移动;
d.增大HCl物质的量,平衡向消耗HCl的方向移动;
(3)a.根据速率之比对化学计量数之比,可以确定v正(H2)=v逆(H2);
b.都表示正反应速率,反应自始至终都成立;
c.混合气体密度保持不变说明混合气体的总质量不变,而平衡移动则气体的质量发生变化;
d.平衡时浓度关系与起始浓度有关、与转化率有关;
(4)该反应正反应是放热反应,降低温度,平衡向正反应移动,到达新平衡,H2的物质的量减小,HCl的物质的量物质的量增大.
解答 解:(1)固体的质量增加了2.80g为Si3N4的质量,其物质的量$\frac{2.8g}{140g/mol}$=0.02mol,根据方程式可知消耗氢气的物质的量=0.02mol×6=0.12mol,故v(H2)=$\frac{\frac{0.12mol}{2L}}{3min}$=0.02mol/(L.min);
平衡常数为生成物浓度化学计量数次数幂之积与生成物浓度化学计量数次数幂之积的比值,故该反应平衡常数K=$\frac{{c}^{12}(HCl)}{{c}^{3}(SiC{l}_{4})•{c}^{2}({N}_{2})•{c}^{6}({H}_{2})}$,
故答案为:0.02;$\frac{{c}^{12}(HCl)}{{c}^{3}(SiC{l}_{4})•{c}^{2}({N}_{2})•{c}^{6}({H}_{2})}$;
(2)a.平衡常数只受温度影响,压强增大,平衡常数K不变,故a错误;
b.正反应为放热反应,升高温度平衡向逆反应方向移动,平衡常数减小,故b正确;
c.Si3N4是固体,增大其物质的量,不影响平衡移动,故c错误;
d.增大HCl物质的量,平衡向消耗HCl的方向移动,即向逆反应方向移动,故d正确,
故答案为:bd;
(3)a.根据速率之比对化学计量数之比,可以确定v正(H2)=v逆(H2),说明反应到达平衡状态,故a正确;
b.都表示正反应速率,反应自始至终都成立,不能说明到达平衡状态,故b错误;
c.混合气体密度保持不变说明混合气体的总质量不变,而平衡移动则气体的质量发生变化,可以说明到达平衡状态,故c正确;
d.平衡时浓度关系与起始浓度有关、与转化率有关,不能说明到达平衡状态,故D错误,
故答案为:ac;
(4)该反应正反应是放热反应,降低温度,平衡向正反应移动,到达新平衡,H2的物质的量减小,HCl的物质的量物质的量增大,新平衡H2和HCl的物质的量之比<$\frac{m}{n}$,
故答案为:<.
点评 本题考查化学反应速率计算、平衡状态判断、化学平衡移动等,意在考查学生的思维能力和分析推理能力,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表:
乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表:| 物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
| 沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;B→C的反应类型是取代反应.
;B→C的反应类型是取代反应. $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +nH2O.
+nH2O. 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若1mL PH=1盐酸与100mL MaOH溶液混合后,溶液PH=7,则NaOH溶液的PH=11 | |
| B. | 在滴有酚酞溶液的氨水中,加入NH4Cl的溶液恰好无色,则此时溶液的PH<7 | |
| C. | 某醋酸溶液的PH=a,将此溶液稀释1倍后,溶液的PH=b,则a>b | |
| D. | 1.0×10-3mol/L盐酸的PH=3.0,1.0×10-8mol/L盐酸PH=8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  表示KNO3的溶解度曲线,a点所示的溶液是80℃时KNO3不饱和溶液 | |
| B. |  表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| C. |  表示0.1000mol/LNaOH滴定20.00 mL 0.1000mol/L醋酸的滴定曲线 | |
| D. |  表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,体积V与沉淀n的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
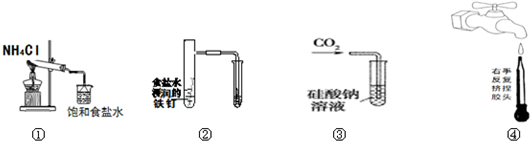
| A. | 实验①制取的氨气溶解在饱和NaCl溶液 | |
| B. | 实验②通过观察右边试管有无倒吸现象说明铁钉是否发生吸氧腐蚀 | |
| C. | 实验③可用于证明碳的非金属性比硅强 | |
| D. | 图④是实验室洗涤胶头滴管的操作 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com