
| A.陶瓷、水泥 | B.单晶硅、玻璃 |
| C.石膏、漂白粉 | D.水玻璃、铝热剂 |
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源:不详 题型:单选题
| A.高纯度的硅广泛用于制作计算机芯片 |
| B.硅可由二氧化硅还原制得 |
| C.低温时,硅与水、空气和盐酸不反应,但能与氢氟酸反应 |
| D.自然界中硅的储量丰富,自然界中存在大量的单质硅 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2CO3比H2SiO3受热易分解 |
B.高温下能发生反应Na2CO3+SiO2 Na2SiO3+CO2↑ Na2SiO3+CO2↑ |
| C.CO2能溶于水生成碳酸,而SiO2却不溶于水 |
| D.CO2通入Na2SiO3溶液中有胶状沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SiC是一种新型无机非金属材料,任何条件下都不可能在空气中燃烧 |
B.制造粗硅时的反应:2SiO2+5C Si+SiC+4CO↑ Si+SiC+4CO↑ |
| C.Si、SiO2能用NaOH溶液分离 |
| D.纯净的SiO2只能用于制造光导纤维 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.C2O3和CO2是同素异形体 | B.C2O3和CO燃烧产物都是CO2 |
| C.C2O3和CO都是酸性氧化物 | D.C2O3和CO2都是碳酸的酸酐 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH(g) △H1=-116 kJ·mol-1
CH3OH(g) △H1=-116 kJ·mol-1| A.使用高效催化剂 | B.降低反应温度 |
| C.增大体系压强 | D.不断将CH3OH从反应混合物中分离出来 |
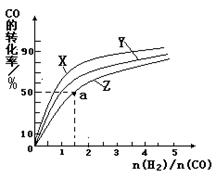
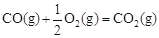 △H2=-283 kJ·mol-1
△H2=-283 kJ·mol-1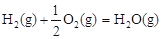 △H3=-242 kJ·mol-1
△H3=-242 kJ·mol-1查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com